乳腺癌研究报告显示导管原位癌的新见解
加州大学戴维斯分校新的研究支持最近假设导管原位癌和浸润性乳腺癌发展相同的乳腺癌的祖细胞。这项研究是国际协会年会上报道乳腺癌研究上个月在蒙特利尔。
“这些研究和其他的含义可能是乳腺癌的基因代码写在癌前期阶段,所以剩下的是注定的,”罗伯特·d·卡迪夫说,病理学教授突变小鼠病理实验室主任在加州大学戴维斯分校比较医学中心。“这对乳腺癌的预防和治疗意义深远。”
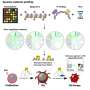
传统信仰是DCIS,最常见的局部乳腺癌,传播超越了乳导管只有DCIS细胞受到额外的基因损害。新假说认为,乳腺癌祖细胞从一开始就存在在癌前病变,并由基因决定进步不仅DCIS,还对浸润性乳腺癌。
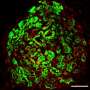
加州大学戴维斯分校的研究结果是基于研究的转基因小鼠乳腺上皮内瘤变,或MIN,鼠标人类DCIS的等效。
小鼠模型,由加州大学戴维斯分校和加州大学圣地亚哥分校的研究人员开发的,只有在加州大学戴维斯分校。
卡迪夫,即将卸任的总统的国际协会乳腺癌研究,总结新假说的证据演讲题为“乳房癌前期:旧的概念和新的生物。”
“新假说表明我们将错误的乳腺癌细胞,”卡迪夫说。“我们需要确定如何正确识别乳腺癌祖细胞在高危妇女和破坏这些细胞才能成为恶性。”
在蒙特利尔会议上,四组加州大学戴维斯分校的研究人员报道了他们在分钟工作,DCIS和小鼠乳腺浸润性癌。
L卡拉韦特三世,生物化学和分子医学副教授加州大学戴维斯分校癌症中心,报告了他的研究作用的物质称为Nrdp1路径对恶性肿瘤。卡拉韦的研究小组发现,当老鼠和人类乳腺癌细胞Nrdp1过剩,生长因子称为ErbB3的水平下降,抑制癌细胞的生长和能动性。同样发生在鼠标ErbB2过剩的乳腺癌细胞。生长因子ErbB2是鼠标对应人类生长因子的HER2,这是涉及人类乳腺癌的四分之一。调查结果显示Nrdp1可能在人类治疗her2阳性乳腺癌的作用。
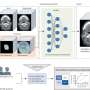
第二个团队报道,最小的看似不可阻挡的发展对乳腺癌细胞在某些情况下可能会停止。劳伦斯领导的团队,年轻,比较医学中心的高级研究助理,和杰夫•格雷格病理学副教授,发现雷帕霉素抗生素快速诱导细胞凋亡,或快速的细胞死亡,在一些但不是全部最小细胞系。研究人员下一步是使用微阵列基因分析,以确定哪些基因表达的幸存的恶性细胞。这些基因可能是有前途的药物开发的目标。
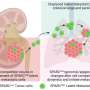
第三个团队提出工作建议,利尿剂可能对DCIS有疗效。史蒂文·安德森,助理研究员在生理学和生物膜,彼得爱定,生理学和生物膜的教授和主席,进行了专门的成像研究表明最小细胞依靠分子称为/钠氢交换器乳导管内保持良好的pH值平衡。利尿剂抑制/钠氢交换,导致酸性致命癌症细胞的微环境。
“这项研究有潜力提供创新治疗高危女性DCIS,“爱说。第四小组报告的方法决定哪些基因在乳腺癌带来恶性肿瘤。Patrizia Damonte,加州大学戴维斯分校的研究者比较医学中心和亚历山大•Borowsky病理学助理教授,拥有单独的最小损伤成单个细胞,每个细胞培养成一个多细胞丛和观察每个丛发展成癌症。他们现在分析的基因构成恶性团。
来源:加州大学戴维斯分校