基因缺陷是肥胖的保护性屏障
梅奥诊所(Mayo Clinic)的研究人员通过对长寿分子线索的研究,找到了另一条可以解释为什么一些摄入过多卡路里的人不会增重的途径。这项研究是在实验室小鼠模型上进行的,指出了一种名为CD38的基因的缺失。当该基因缺失时,高脂肪饮食的小鼠体重不会增加,但当该基因存在时,小鼠会变得肥胖。
这些发现发表在本月的《FASEB期刊》网络版上,这是美国实验生物学学会联合会的期刊。这项研究将发表在2007年11月的杂志印刷版上。
“肥胖是一个由多种因素造成的复杂问题,其中之一就是我们的基因。基因在大约50%的病例中起作用,在这项研究中,我们证明了CD38调节体重,”梅奥诊所的麻醉师、该研究的通讯作者爱德华多·奇尼(Eduardo Chini)博士说。
奇尼博士说,找出导致高脂肪、高热量饮食导致肥胖的信号机制,是理解和开发新的肥胖治疗方法的关键部分。
对动物模型的研究表明,限制卡路里可以降低胆固醇和血压,这两项指标通常被认为是衰老的生物标志物。此外,已发表的动物模型研究表明,热量限制(定义为每天摄入比平均摄入量少30%至40%)可以打开SIRT1基因,这是与长寿有关的七个基因家族之一。
此外,最近的研究表明,化学受体PGC1(过氧化物酶体增殖物激活受体辅激活物)在肥胖的发生和代谢控制中起着关键作用。SIRT基因激活PGC1,这样做可以抵消肥胖的负面影响——至少在老鼠身上是这样。但是SIRT-PGC1反应是如何起作用的,直到现在还没有完全解释清楚。
在梅奥诊所研究团队之前的实验室研究中,CD38被证明参与调节多种信号通路,例如调节能量代谢的信号通路。此外,最近对人类的研究也表明CD38与代谢,特别是代谢综合征之间可能存在联系。代谢综合征包括与代谢相关的健康问题,通常困扰肥胖人群。这些健康问题包括高血压、胰岛素水平升高和高胆固醇水平。
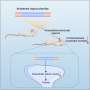
在这项研究中,研究人员调查并证实了CD38在小鼠模型中抑制SIRT和PGC1的表达,从而调节体重。在缺乏CD38的情况下,SIRT-PGC1通路被激活,并保护小鼠模型免受肥胖的影响。
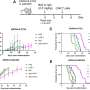
研究人员研究了两组小鼠:一组带有CD38基因,另一组没有。每组都被喂食高热量饮食,其中60%的卡路里来自脂肪。在第二项测试中,每组都被喂食标准饮食,其中4%的卡路里来自脂肪。
结果,携带CD38的高脂饮食小鼠的体脂几乎增加了四倍,体重几乎增加了一倍。在高脂肪饮食八周后,带有CD38的小鼠开始出现葡萄糖耐受不良的迹象,这是糖尿病发病的第一个指标之一。此外,这组老鼠只活了4到6个月,而第二组老鼠活了12个月。
对于没有携带CD38的那组老鼠来说,即使它们吃高脂肪食物,它们的体脂和体重也没有变化。这些老鼠燃烧了更多的能量,更苗条,在其他方面也更健康。
“这些变化有助于这些小鼠在高脂肪饮食和缺乏锻炼的情况下抵御体重增加的能力。总之,这些结果表明CD38缺乏对高脂肪、饮食引起的肥胖具有保护作用,”Chini博士说。
奇尼博士及其同事还研究了白藜芦醇对小鼠的影响。白藜芦醇是一种天然存在的物质,存在于桑葚、花生和用于酿酒的红葡萄等植物中。尽管缺乏证据表明白藜芦醇对人类安全有效,但它被作为一种模仿适度运动效果而不进行体育锻炼的药物销售,也被作为一种长寿药物销售。
携带CD38的小鼠每天服用30毫克(mg)白藜芦醇。为了确定SIRT基因对肥胖的影响,没有CD38的小鼠接受了相同剂量的sirtinol,一种可以关闭SIRT基因的药物。
研究人员发现,带有CD38的小鼠在接受白藜芦醇治疗两周后,可以避免高脂肪、饮食引起的肥胖。相比之下,sirtinol对小鼠在缺乏CD38的情况下对高脂肪、饮食诱导的肥胖的保护作用无效。用sirtinol治疗的没有CD38基因的小鼠与没有使用sirtinol治疗的没有CD38基因的小鼠相比,体重增加了统计学意义上的显著量。
这一数据支持了CD38通过SIRT依赖机制调节高脂肪、饮食诱导的肥胖的新观点。
作者写道:“这些结果共同确定了一种调节体重的新途径,并清楚地表明CD38是导致饮食诱导肥胖的细胞级联反应中几乎必不可少的组成部分。”
作者说,这项研究的结果很有希望,应该在后续研究中进行探索,这些研究将重点放在小鼠的生活质量和寿命上。
资料来源:梅奥诊所