研究人员试图让导致蛀牙的细菌自我毁灭
更大的目标是消除关键酶对所有链球菌和葡萄球菌疾病的贡献
那些吃糖并释放导致蛀牙的酸到牙齿上的细菌可能很快就会对它们自己的酸变得非常脆弱。研究人员已经确定了关键基因和蛋白质,如果这些基因和蛋白质受到干扰,就会夺走一种关键细菌的繁殖能力,因为酸性废物会在口腔中积聚。
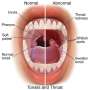
变形链球菌(S. mutans)在酸性环境中生存的能力是该物种成为全球蛀牙主要驱动力的原因之一。过去的研究表明,这种能力有几个组成部分,包括一种叫做脂肪酸生物合成酶M (FabM)的细菌酶,当这种酶被关闭时,变形链球菌对酸的伤害几乎是原来的1万倍。
此外,早期的研究表明,FabM或其亲属之一也可能帮助所有链球菌和葡萄球菌感染抵抗人体的防御系统,其中包括使细菌遭受酸的免疫细胞。在它们之间,“链球菌”和“葡萄球菌”是脑膜炎、肺炎、败血症、耐甲氧西林金黄色葡萄球菌、“食肉”感染(筋膜炎)以及心脏瓣膜和支架周围感染的罪魁祸首。
虽然FabM是新药设计的主要目标,但下一轮工作的重点是识别和排序2000个已知变异链球菌基因中的每一个基因,这些基因有助于变异链球菌的“适应性”(生存、竞争其他菌株和致病的能力)。罗切斯特大学医学中心的一个研究小组今天宣布,它已经从美国国立卫生研究院(NIH)下属的国家牙科和颅面研究所(NIDCR)获得了360万美元的健康状况分析拨款。拨款资助的项目将寻求创建一个蛋白质目录,与FabM一起,可以作为多管齐下攻击细菌的目标,这些细菌往往围绕单推力处理进化。
罗彻斯特大学医学中心微生物学与免疫学教授、该基金的首席研究员罗伯特·g·奎维博士说:“我们的第一个目标是迫使导致蛀牙的主要细菌在吃糖后立即用自己的酸来摧毁自己。”“在那之后,这项工作可能有助于为许多已经对抗生素产生耐药性的感染带来新的抗菌联合疗法。”
研究细节
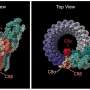
2002年,圣裘德儿童研究医院传染病科的教员查尔斯·o·洛克博士发表了他的研究,描述了FabM酶的存在。Rock是Quivey基金申请的顾问,他还确定了FabM基因在链球菌膜中脂肪酸化合物的构建中所起的作用,这是它们对周围世界的一种屏障。Quivey和同事首次将FabM方法应用于口腔疾病,大约两年后,他们发表了一项研究,表明FabM酶是构成变形链球菌膜的脂肪酸在酸性增加时发生巨大变化的原因。
变形链球菌产生乳酸作为发酵的废物,一些古老的生命形式在不使用氧气的情况下将糖转化为生命所需的能量。经过许多代的暴露在自己的酸性废物中,这个物种的膜已经变得“耐酸”。Quivey的团队已经证明,FabM通过使碳链(变形链球菌膜脂肪酸的主要功能特征)变长来促进这种持久性。事实上,随着酸度的增加,细菌外膜中多达60%的脂肪酸会发生这种变化,Quivey说。
研究人员已经证明,这种结构变化可以保护细胞膜,可能是通过使酸更难向细胞膜提供氢离子,但他们还不知道原因。使氢离子作用于其他化合物使酸有了坏名声。剩下的问题,该团队将寻求解决在未来五年内,包括如何在膜长脂肪酸专门防止酸,以及细菌如何感知酸度的变化。
为了帮助回答这些问题,Quivey的团队对第一个也是唯一一个去除FabM基因的变形链球菌进行了基因工程改造。
这种FabM“击倒”突变体是一个活的模型,显示了酶在活细菌中的确切影响。没有FabM,突变体的外膜充满了其他更小的脂肪酸,这些脂肪酸的耐酸性比通常通过FabM产生的要低得多,但仍然提供了一些抗酸的保护。因此,我们的目标是设计一种治疗方法,防止变形链球菌同时形成直链脂肪酸和“小链”脂肪酸。
Quivey等人正在设计下一代抗菌药物,他们不仅在寻找一种方法来阻止一种致病酶的作用,还在寻找如何关闭它的三四个备份系统。切断细菌基因逃脱途径的过程适用于对细菌生存和致病能力至关重要的每一个特征。除了耐酸能力外,研究小组还将研究变异链球菌能够通过产生含糖聚合物(菌斑)粘附在牙釉质上的基因和蛋白质。蛀牙是牙菌斑与酸结合的结果。
Quivey在拨款申请中的合作伙伴是生物化学和生物物理学研究副教授Elizabeth Grayhack博士,微生物学和免疫学教授Robert Marquis博士,生物化学和生物物理学教授Eric Phizicky博士。Quivey说,NIH的拨款申请获得了成功,因为该团队和提案结合了多年的基因组项目经验(Grayhack和Phizicky)和丰富的微生物经验(Marquis和Quivey)。
作为拨款的一部分,Grayhack和Phizicky将为已知的2000个突变S. mutans基因创建一个突变菌株库,每个菌株只关闭了2000个基因中的一个。例如,他们将把这些库放入酸中,看看哪些菌株能茁壮成长。知道了每个菌株中缺失的基因,研究人员就能得出关于每个基因不仅对耐酸性的贡献,而且对链球菌生存和致病能力的许多方面的贡献的结论。
马奎斯说:“在这条道路上,建成的图书馆将使研究人员能够确定与口腔疾病有关的每一种细菌蛋白质,了解它们的确切结构,并定制出干扰它们的药物。”“该团队的策略是识别和关闭细菌可能抵抗治疗的四种主要方式。”
资料来源:罗切斯特大学医学中心