毒性机制确定帕金森病
路易小体的神经学家观察到几十年,几块聚合的蛋白质在细胞内,出现在帕金森氏症患者的大脑和其他神经退行性疾病。
路易小体的存在表明蛋白质回收和废物处理潜在的问题,导致了困惑:如何影响这些过程杀死脑细胞?
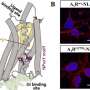
一个可能的答案是:打破一个叫做MEF2D生存电路。埃默里大学医学院的研究人员发现,MEF2D路易小体的主要成分敏感,一种叫做α-突触核蛋白的蛋白质。
在帕金森病细胞培养和动物模型,α-突触核蛋白的积累MEF2D干扰细胞的回收,导致细胞死亡。MEF2D尤其丰富的帕金森症患者的大脑中,研究人员发现。
研究结果将发表在1月2日,2009年科学。
“我们发现这可能是控制细胞损失和生存的一个重要途径在帕金森病,“说毛Zixu资深作者,博士,埃默里大学医学院药理学副教授。
进一步的研究可以确定药物,可以调节MEF2D,使大脑细胞生存有毒强调损害蛋白质回收,他建议。
大多数情况下的帕金森病称为零星的,这意味着没有明显的遗传原因,但也有继承形式的帕金森氏症。其中的一些可以与α-突触核蛋白基因突变或基因的三倍。突变和三倍使大脑产生一种有毒的α-突触核蛋白或α-突触核蛋白比正常。
”在某种程度上是有毒的,但是α-突触核蛋白并不是生存和死亡的细胞的机械的一部分,”毛说。
他和他的同事开始研究α-突触核蛋白如何影响MEF2D在处理另一个实验室的一份报告后的α-突触核蛋白即使伴娘自噬(CMA)。
在CMA,某些选定的蛋白质注入溶酶体,隔间的细胞用于咀嚼废弃蛋白质。毛和他的同事们发现,溶酶体与细胞会吸收MEF2D蛋白质,和干扰CMA化学原因MEF2D水平上升。
MEF2D是一个转录因子,一种蛋白质控制多个基因是否开启或关闭。先前的研究显示MEF2D需要适当的发展和大脑细胞的生存。函数,MEF2D必须能够结合DNA。
作者发现CMA中断时,大部分的累积MEF2D不能绑定DNA。这可能表明,蛋白质折叠不当或修改。
“尽管有很多的东西是让MEF2D蛋白质不活跃,”毛说。
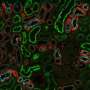
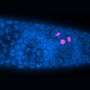
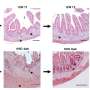
毛和他的同事们发现,老鼠,人为过度生产α-突触核蛋白(帕金森病模型)的水平会升高明显不活跃MEF2D在他们的大脑。此外,MEF2D蛋白质含量更高在帕金森病人的大脑控制。
影响后的α-突触核蛋白MEF2D可能是路上连接的各种遗传和环境危险因素帕金森,即使CMA不是唯一的机制,毛说。
“这可能是各种压力影响MEF2D以不同的方式,”他说。“我们认为这项工作提供了一个解释,几个重要的观察结果联系在一起的。”
参考:杨问。,et al .,调节神经元生存因素MEF2D即使伴娘自噬,科学,2009年1月2日。
来源:埃默里大学