罕见的遗传性疾病帕金森病提供了独特的见解
马萨诸塞州综合医院调查似乎发现之前报道背后的机制之间的联系罕见遗传病戈谢病和帕金森病常见的神经退行性疾病。在一份报告中出现在7月8日出版的细胞和接收早期在线发布,他们描述分子通路中断导致戈谢病导致有毒的神经元沉积蛋白质的α-突触核蛋白(α-syn)发现在帕金森病及相关疾病。另外,α-syn水平上升进一步抑制高雪氏症相关的通路,导致更α-syn沉积,这一发现表明针对这一途径可能是治疗帕金森症患者的新选项。
“我们的发现表明,这个分子通路不仅适用于高歇氏患者和他们的亲属,他们中的一些人可能有帕金森病症状,患者也常见的帕金森氏症或其他synucleinopathies,“迪米特里Krainc说,医学博士,博士的大众婴幼儿专科研究所神经退行性疾病(MGH-MIND),这项研究的资深作者。“看来α-syn沉积之间的交互和高歇氏通路形成一个反馈回路,最终导致自动传输的疾病。”
在戈谢病主要发生在儿童,病人承受两个不活跃的基因编码酶的副本葡糖脑苷脂酶(GCase),分解脂质分子称之为物质(相关)。缺乏功能性GCase导致积累相关水平的细胞被称为溶酶体的小隔间里,细胞废料通常消化。相关积累在器官如肝脏、脾脏、骨髓,有时大脑,导致高歇氏的症状,这通常是由静脉注射治疗替代失踪GCase的酶。
临床观察表明高歇氏之间的连接和帕金森病,影响一百万成年人在美国一些高歇氏患者或其亲属与单个缺陷的副本GCase基因也出现典型的帕金森症状的震颤,肌肉僵硬和缓慢的移动。此外,病人患有零星的帕金森病也可能在GCase基因突变。事实上,突变基因是目前最常见的帕金森病的遗传风险因素。没有以前的研究,然而,直接检查如何GCase突变导致帕金森病的症状。
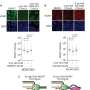
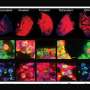
MGH-MIND研究团队发现,突变降低GCase导致过剩的表达相关脂质在培养的神经元。通过与α-syn互动,这些相关脂质引起的积累蛋白质。脑组织样品从高歇氏的小鼠模型和高歇氏或帕金森患者相关疾病证据还显示连接减少GCase表达神经元α-syn沉积增加。在培养细胞和动物和人类的样本,α-syn存款也与神经退化。
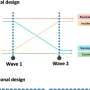
其他研究表明,过度的α-syn可能会干扰细胞内蛋白质的正常处理,MGH-MIND团队也研究了α-syn如何影响细胞内GCase的运动和活动。他们发现α-syn积累会干扰溶酶体功能通过减少GCase的活动。这种交互α-syn和GCase之间形成一个反馈循环,达到某一阈值后,可能会导致自动传输的疾病。
“我们现在建议疗法针对葡糖脑苷脂酶活动可能有助于打破α-syn积累和神经退化的恶性循环,”Krainc说,哈佛医学院的神经病学副教授。“我们认为这个途径适用于任何潜在的疾病,其特征是α-syn积累,现在与产业合作开发新的治疗方法帕金森病提高目标葡糖脑苷脂酶的溶酶体。我们希望这种疗法可能预防或减少α-syn的积累和合成神经退化疾病如帕金森氏症和老年痴呆症的路易小体”。