发现kras突变结肠癌的潜在治疗靶点
来自麻省总医院(MGH)癌症中心的研究人员已经确定了一种新的潜在策略,用于治疗KRAS基因突变驱动的结肠肿瘤,这种肿瘤通常抵抗传统和靶向治疗。在2月17日出版的《细胞研究小组报告说,针对KRAS激活到肿瘤生长的通路中的一个后期步骤可能能够阻止这一过程。
“并不是所有kras突变结肠癌都是一样的,”丹尼尔·哈伯医学博士说,他是MGH癌症中心主任,也是该研究的共同通讯作者细胞报告。“大约一半的人似乎非常依赖KRAS突变来生存,而另一半人即使在KRAS被抑制的情况下也能继续生长。在kras依赖的肿瘤中,我们确定了突变如何增强a通路众所周知,它与结肠癌有关,并确定了通往该途径的关键步骤,如果抑制该途径,可以诱导kras依赖肿瘤细胞发生细胞凋亡或程序化细胞死亡."
激活KRAS表达的突变在一些疾病中很常见癌症类型-最常见的是结直肠癌和肺癌-已知表明治疗耐药性。直接针对KRAS活性的药物还没有成功,并且试图确定其他潜在的靶点一直具有挑战性,因为KRAS突变可能在不同的癌症中起不同的作用。MGH团队首先着手确定kras突变肿瘤的百分比,这些肿瘤的生长依赖于突变的存在。
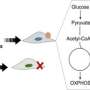
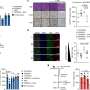
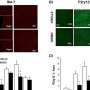
对大量kras突变肿瘤细胞系的分析显示,当kras表达被阻断时,大约一半的肿瘤细胞系会死亡。对kras依赖肿瘤的更详细分析发现了几种过表达基因,并发现阻断生长因子相关酶TAK1的表达是诱导肿瘤细胞死亡的最有效方式。研究人员随后证明,用TAK1抑制剂治疗会导致培养的kras依赖性细胞死亡结肠癌并减少了植入小鼠皮肤下的kras依赖肿瘤的大小。进一步的研究表明,KRAS激活通过涉及TAK1和信号分子BMP的途径促进肿瘤的发展,这有助于增强已知参与胚胎发育和癌症的Wnt途径。
哈伯说:“并不是所有在癌症中突变的基因都可以被药物直接靶向,但这项研究表明,如果你了解特定类型肿瘤中所有信号通路之间的相互关系,你可能会发现一个漏洞,让你绕过‘不可药的目标’。”哈伯是哈佛医学院肿瘤学教授库尔特J. Isselbacher/Peter D. Schwartz,也是霍华德休斯医学研究所的研究员。
Haber补充说:“我们在这项研究中使用的TAK1抑制剂不适合人类给药,但制药公司有小分子TAK1抑制剂尚未开发出来,因为它们的潜在应用尚不清楚。”“现在我们需要确定剂量水平,使这些或相关药物能够对抗kras依赖性结肠癌而不具有毒性。这些研究,结合对这一途径的机制和抑制其后果的更好理解,将使我们更接近临床试验的规划。”