鉴定出未检查的血管生成后面的罪魁祸首
德国研究人员阐明了控制血管生长的关键调节机制,这可能有助于解决将来的耐药性问题。
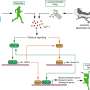
血管生成是新血管的生长,是一个复杂的过程,在此过程中,不同的信号蛋白以高度协调的方式相互相互作用。生长因子VEGF和Notch信号通路都在此过程中起重要作用。VEGF通过与其受体VEGFR2结合来促进血管的生长,而Notch信号通路的作用就像能够抑制血管生成的开关。直到最近,科学家还是假设Notch通过下调VEGFR2取消VEGF的影响。现在,研究人员马克斯·普朗克分子研究所生物医学德国穆纳斯特的Westphalian Wilhelm-University能够证明,即使抑制了VEGF或VEGFR2,有缺陷的Notch信号也可以强大而放松管制的血管生长。在这种情况下,不同的VEGF家族受体VEGFR3强烈上调,促进血管生成。“这一发现可能有助于解释耐药性MPI组织生物学和形态发生部门主席Ralf Adams建议,某些类型的癌症治疗问题可能成为新型治疗策略的基础。
一个广泛的分支血管网络为人体的每个器官提供营养,并从组织中去除有害的代谢废物产品。这种血管系统的生长对于发育和伤口愈合过程至关重要。不受控制的血管生成有助于血管瘤,皮肤中血管样的血管瘤过度生长,或者会损害糖尿病和老年人视力的视网膜病变。在癌症治疗中,使用血管生成的抑制作用用于饥饿肿瘤并防止通过循环系统癌细胞的转移扩散。目前,这是最常通过靶向VEGF或其受体VEGFR2完成的。当它们的氧气供应不足时,组织开始释放与VEGFR2结合的VEGF,激活受体,从而触发血管生长。因此,可以通过抑制VEGF或VEGFR2阻断新血管的形成。不幸的是,现有的治疗不足,由于尚不清楚的原因,有些患者对VEGF/VEGFR2抑制作用反应不佳或没有反应。
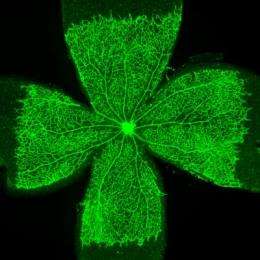
现在,亚当斯部门的博士后研究员鲁·贝尼迪托(Rui Benedito)表明,即使抑制了VEGF或VEGFR2,小鼠眼容器中对缺口途径的抑制也允许强大和放松管制的血管生长。贝尼迪托解释说:“事实证明,另一个VEGF家族受体VEGFR3接管了促进新血管的形成。”VEGFR3强烈上调血管在没有凹槽的情况下,即使没有周围组织的生长信号,也很活跃。
“我们现在需要做的是确认VEGFR3和其他Notch调节的信号实际上是否能够促进vegf无关血管生长亚当斯解释说,不仅在小鼠的眼科或癌症中,而且在人类中也是如此。这将使医生在必要时选择替代疗法。在这里,MPI,医学院和Münster大学之间的合作也至关重要:“我们的工作从大学提供的出色支持中受益匪浅。”
进一步探索