在药品批准竞赛中,美国FDA在加拿大,欧洲
通常美国食品和药物管理局(FDA)批准药物疗法更快,比其在加拿大和欧洲同行,根据一项新的研究,耶鲁大学医学院的研究人员。研究计数器的看法,药物审批过程在美国特别慢。
由二年级医学生尼古拉斯·唐宁和资深作者约瑟夫•罗斯医学博士,assistant professor of internal medicine at Yale School of Medicine, the study will be published May 16 online by the新英格兰医学杂志》上。
监管审查代表最后一步的过程中带来新的医疗技术从实验室到床边。有效的监管审查过程可以使病人更快获得有前途的新疗法,同时确保药品安全。
“认为FDA太慢意味着病人不必要的等待监管机构完成新药申请的审查,”唐宁说,决定进行这项研究,因为没有最近比较FDA的监管审查速度与在其他国家监管机构。
唐宁、罗斯和同事回顾了FDA药品批准决定,加拿大药品监管机构健康加拿大和欧洲药品局(EMA)在2001年和2010年之间。他们研究了每个监管机构的药品审批的数据库来识别小说疗法以及关键管理事件的时间,允许监管审查速度计算。加拿大和欧洲被选作比较,因为他们都面临着同样的压力批准新药快速的同时确保他们不要把病人处于危险之中。
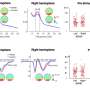
研究小组发现,总时间中位数在FDA审查是322天,366天在加拿大卫生部EMA和393天。
“子样品中药物三个监管机构批准,FDA审查结束了快3个月比加拿大教育津贴或健康,”唐宁说。“FDA的总复习时间快于EMA,尽管FDA更高比例的应用程序需要多个监管审查。”
唐宁说,大多数新药物治疗首先在美国批准使用“检查小说药品批准在多个市场,我们发现64%的药品批准在美国和欧洲批准美国病人第一,和86%的药品批准在美国和加拿大也批准了第一个在美国”,他说。
更多信息:新英格兰医学杂志》上,doi: 10.1056 / NEJMoa1200223