在免疫细胞的职业道之后
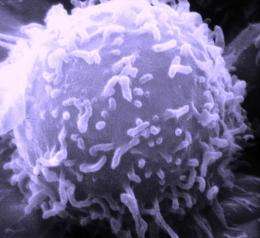
免疫系统产生不同品种的T细胞(图1),例如病原体破坏细胞毒性T细胞和免疫应答升压辅助T细胞。监管T(treg)细胞抑制这些其他细胞并防止身体反应过度威胁或产生危险的自身免疫反应。
T.reg细胞通常通过表达转录调节蛋白Foxp3的表达鉴定,但横滨中瑞肯Hori的团队的新工作已经证明这不是可靠的签名。
几个组获得了数据,表明Treg细胞可以基本上“改变职业”,丢失其Foxp3表达并转化为其他T细胞类型。然而,来自Hori和同事的调查结果导致他们提出替代的“异质性模型”。“我们的观察结果表明,这些现象可以通过福索普3 + T细胞的未成年人的群体完全解释,而不假设重新编程,”他说。他的小组现在已经通过使用标签技术为这一假设提供了令人信服的证据,使它们能够区分目前表达Foxp3的细胞,而不是在过去表达该蛋白质。
研究人员鉴定了两组表达对表达的细胞,其对免疫刺激不同的反应。最稳定地表达该蛋白质,并且在高水平下表达,并且表现出T的功能特征reg细胞。少数群体分数显示Foxp3表达的瞬态爆发,但最终发展到其他T细胞类型。这些'exfoxp3'细胞似乎没有代表重编程的treg细胞,而是单独的T细胞库,其仅均匀地产生该蛋白质。
有趣的是,他的团队也了解到一些reg细胞确实进入一个状态,他们停止表达foxp3,尽管它们会保留他们的身份的“记忆”reg细胞。这是通过对编码Foxp3的基因内的DNA的化学修饰来实现,并且免疫刺激及时导致强大的重新表达蛋白质。“这应该强迫人们重新考虑Foxp3的流行而过度简化视图作为T的主监管机构reg细胞,“Hori说。
因此,确定该表达谱的事件可能在建立比Foxp3的存在或不存在的情况下,在建立细胞身份方面可能证明更重要。“已经推测了Treg血统是由富索上游的高阶监管途径决定,但该系统的性质是未知的,“Hori说。在未来的工作中,他计划与其他riken实验室的同事合作,更密切地调查这个问题。
进一步探索
小松,N.等人。天然Foxp3 + T细胞的异质性:一种犯下的调节T细胞谱系和未提交的轻微群体保持可塑性。国家科学院的诉讼程序106,1903-1908(2009)。








用户评论