抑制CaMKII酶活性可能导致心脏疾病的新疗法
爱荷华大学的研究人员曾表明,一种叫做凸轮激酶的酶II中起着举足轻重的作用在心脏病发作后心脏细胞的死亡或其他条件,心肌损伤或压力。失去心脏细胞通常是永久性的,会导致心脏衰竭,严重衰弱状态,影响580万人在美国。
现在UI团队,由马克•安德森医学博士博士,教授和内科医学主管UI Carver医学院,在如何磨练凸轮激酶II触发心脏细胞死亡后心脏损伤,表明动作发生在线粒体细胞的能源生产。在动物实验中,研究小组报告说,阻止酶可以防止心脏细胞死亡,和保护动物的心脏衰竭。
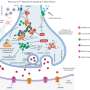
线粒体是细胞的电池,产生细胞的能量需要。在心脏细胞、能源生产的这些小蜂窝组件每个心跳燃料。然而,当心脏压力,例如心脏病发作期间,线粒体成为漏水和非功能性,从而触发细胞死亡和心脏衰竭。
“我们发现活动的凸轮激酶二世在线粒体酶促进细胞死亡时强调,“美玲乔伊纳说,博士,UI内科医学助理教授、该研究的第一作者,这是10月10日在线发表在《华尔街日报》自然。“这些发现可能会帮助我们推进治疗心脏疾病,减少心脏病发作后死亡率。”
新的研究表明,激活第二凸轮激酶促进线粒体的泄漏和增加心肌损伤通过允许过多的钙进入线粒体。具体来说,UI团队发现第二凸轮激酶调节钙进入线粒体通过修改一个特殊的线粒体钙通道。过多的酶活性增加钙流入线粒体的数量,这钙超载触发细胞死亡。
使用转基因小鼠,研究小组还显示,抑制第二凸轮激酶活动阻止线粒体钙超载,减少线粒体中断,和保护的老鼠心脏细胞死亡在心脏病发作。
这些发现为线粒体功能和提供洞察分子机制表明,抑制第二凸轮激酶酶线粒体可能导致新的和更有效的治疗常见的形式心脏病。
“因为线粒体也扮演了一个重要的角色在大脑和骨骼肌其他疾病,例如,我们的研究结果也可以理解和治疗进行非心脏疾病的广泛影响,”安德森说,他也是UI心血管研究中心主任。