突变组蛋白蛋白质机制揭示儿童脑癌
(bob游戏医疗Xpress)大多数癌症治疗是钝的。为了消除肿瘤,肿瘤学家们并非放疗或化疗,可损害健康组织和肿瘤生长。新的研究从c·洛克菲勒大学大卫·阿莱的实验室可能让科学家更接近设计可以精确的目标肿瘤癌症疗法。
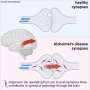
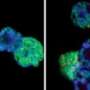
他们的发现,今天在线发表科学快讯,遵循最近的一系列发现几个国际基因组测序财团直接链接一个突变组蛋白蛋白质一种罕见的儿童脑干肿瘤称为DIPG。总的来说,这些研究代表科学家第一次与组蛋白突变疾病,和彼得·刘易斯的兴趣的研究助理alli的染色质生物学和表观遗传学实验室,负责这些新的研究。
结合DNA,组蛋白组成的基因包装材料称为染色质。突变发生在组蛋白H3,涉及到非常具体的一个氨基酸替换,蛋氨酸,另一方面,赖氨酸,在关键位置上的组蛋白尾巴,“沉默”相关的基因。通常情况下,基因沉默产生酶甲基转移酶时,包含一组结构区域称为域,高度赖氨酸的甲基化工集团在位置27 H3尾巴。这种高度特定的化学反应,称为甲基化,是被替换的赖氨酸和蛋氨酸,导致基因监管不力一样。
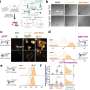
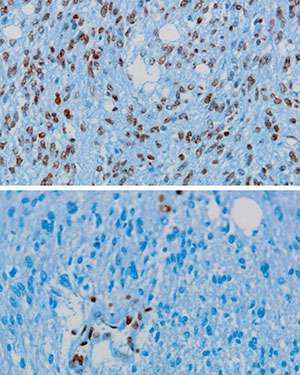
刘易斯和他的同事们看着人类DIPG肿瘤包含methionine-to-lysine替换和确定突变组蛋白H3由3.6%到17.6%的总H3 DIPG样本。他们还发现了一个全球减少正常H3组蛋白的甲基化水平当添加了少量的突变H3正常人类细胞。
“我经常说,每个氨基酸组蛋白问题,”阿莱说,谁是快乐和杰克Fishman教授。“这些研究强调事实。”
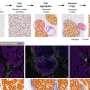
研究人员证明了降低正常H3组蛋白的甲基化结果的干扰活动甲基转移酶叫PRC2突变组蛋白。PRC2导致压迫正常H3的甲基化的基因参与细胞生长途径。没有甲基化基因在这些途径可能成为激活,在DIPG促进肿瘤的生长。艾莉和刘易斯收到了来自美国国立卫生研究院的资助和斯塔尔癌症财团。主要合作者这项工作包括奥伦比结杜克大学医学中心和汤姆缪尔普林斯顿大学和他们的同事。
“我们的发现为我们提供了一个有用的工具来探索生物过程,”刘易斯说。“这也告诉我们如何抑制酶,这可能导致药物的发展,模仿这些突变体的行动。”
“我们现在有一个模式促进脑干肿瘤通过异常的表观遗传沉默突变PRC2,组蛋白的抑制,”阿莱说。“我们已经发现了一个可能有用的机制完全抑制个人SET-domain甲基转移酶,和其他可以想象chromatin-modifying酶在内的各种恶性肿瘤。”
更多信息:刘易斯,p . et al .抑制PRC2活动功能获得的H3突变儿科胶质母细胞瘤中发现,科学在线:2013年3月28日。www.sciencemag.org/content/ear…3/27 / science.1232245