'RNA海绵'机制可能导致ALS / FTD神经变性
最近鉴定了ALS(肌萎缩外硬化硬化)和FTD(胎儿痴呆)的最常见的遗传原因是基因C9ORF72中的改变。但是,突变如何导致神经变性疾病出现神秘。埃默里大学医学院的研究人员已经证明,这种ALS / FTD突变可能有害,因为它产生了“RNA海绵”,浸泡了一种结合RNA的重要调节蛋白质。
结果在线在线公布了国家科学院的诉讼程序,早期版。
“我们认为RNA本身是疾病机制的一部分,”埃默里大学医学院神经内科助理教授的助理托马斯Wingo,MD联合作用。“在细胞文化中和果蝇,我们能够表明我们可以加入由RNA耗尽的蛋白质并改善问题。“
该发现提供了对ALS和FTD的疾病机制的洞察,这两者都在C9ORF72改变和在其他情况下。它表明某些形式的Als / FTD可以具有常见的元素,其具有由非编码重复引起的其他神经变性障碍,例如肌肌营养不良,纺丝术共济失调和脆弱的X相关震颤/共济失调综合征。
高级作者是彭锦,博士,教授人类遗传学在埃默里大学医学院。第一作者是前研究生,Zihui Xu,博士,现在在华中科技大学,研究专家Mickael Poidevin。
Als是一种致命的疾病,其中脑和脊髓脱泥的运动神经元。随着疾病的进展,患者失去了行走,谈话和呼吸的能力。FTD是一种痴呆症的形式,其中患者主要经历行为,人格或语言的恶化。
许多神经根学家和研究人员认为这些条件是共享临床和病理特征。几种基因中的突变与ALS和FTD都相关联,这表明它们具有共同的机制。然而,大多数病例被认为是零星的,这意味着他们没有明确的家族史。
2011年,在C9ORF72中确定了突变,作为最常见的遗传原因ALS和FTD,占每种疾病病例的5%至7%。突变似乎没有影响C9ORF72编码的蛋白质。相反,它扩展了一种重复性DNA,使得序列“GGGGCC”重复在编码蛋白质的基因部分之外的数百次。
这看起来类似于其他神经变性障碍,例如肌肌营养不良,纺丝大脑营养不良和脆弱的X相关震颤/共济失调综合征的“非致重复”扩展。
一些研究人员报道,GGGGCC重复产生转化为在细胞中聚集的异常蛋白质的RNA。这些蛋白质聚集体被认为对神经元有毒。Emory研究人员有另一种解释:GGGGCC重复RNA本身是有毒的。
埃默里团队测试了生产GGGGCC重复RNA的影响,该反复RNA对培养的哺乳动物神经元细胞进行了毒性,并导致果蝇中的神经变性。当在苍蝇的电动机神经元中产生重复RNA时,苍蝇的电动机活性降低。
重复RNA似乎有害,因为当过度引发时,它螯合称为PURα的蛋白质,其粘在GGGGCC重复上。科学家曾发现PURα是神经元发展所必需的,并且参与神经元中RNA的运输。发现神经元细胞或苍蝇产生更多PURα以补偿RNA造成的毒性,埃默西科学家发现。
“对于ALS和FTD,这表明靶向毒性RNA本身或其与PURα的相互作用的抗病策略,”Jin说。“它还提示存在普遍基于RNA的机制,有助于几种神经变性疾病。”
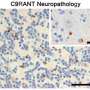
螯合PURα似乎导致受ALS / FTD影响的患者的神经元内的再分分配。Emory团队能够检测含有C9ORF72突变的个体的脑组织样品中的含有Purα的含糊的“包合物” - 以及其他具有FTD但没有C9ORF72突变的个体。
进一步探索












用户评论