压抑的并发症疟疾寄生虫抗原吸收来自免疫反应血管

大多数死亡由疟原虫引起的恶性疟原虫造成脑型疟疾的发病。当寄生虫就会出现这种严重的神经疾病积累在大脑血管。无数的研究多年来,使用鼠标模型实验脑型疟疾(ECM),也表明,宿主免疫细胞中起到关键作用。
先前的研究从* *新加坡Laurent Renia免疫学网络已高亮显示的杰出贡献被称为细胞毒性T淋巴细胞(ctl)细胞。他的团队已经发现了这些细胞促进ECM的机制。ctl通常负责摧毁癌症或感染细胞,但是研究人员怀疑ECM可能源于parasite-targeting ctl也攻击和伤害大脑的血管。
Renia和检测这些ctl及其同事开发的工具靶细胞。然后确定小鼠感染鼠安卡(PbA),一个ECM-causing寄生虫亚型,特别引起ctl针对特定parasite-derived蛋白质多肽块。小鼠感染PbA开始生产ctl承认这种多肽在五天,这些细胞迁移到大脑不久之后。研究人员还研究了三种疟原虫株不触发ECM和惊奇地发现,这些引起了类似的CTL反应。
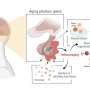
仔细检查从受感染的老鼠的大脑血管显示缺失的拼图的。红细胞被ECM-causing寄生虫感染表现出倾向于积累在这些船只,而从non-ECM-causing寄生虫不。Renia和同事确定,当发生这种积累时,这些血管内皮细胞吸收,然后通过一种机制显示CTL-targeted寄生虫蛋白质称为“cross-presentation”。
这些cross-presenting细胞随后成为CTL-mediated破坏目标,创建泄漏给疟原虫进入大脑。重要的是,提示抗疟药物治疗可以迅速明确这些寄生虫的血管,从而防止ECM的发作。
Renia推测ECM特别来自疟原虫物种具有一些固有的特性,使感染细胞“粘性”。“我们感到惊讶,这细微的差异在寄生虫生物学的封存与non-sequestration导致病理如此巨大的差异,”他说。尽管存在其他已知的例子内皮cross-presentation机制仍然知之甚少。Renia渴望发现疟原虫如何将免疫应答。“这是一个有趣的生物学问题,因为内皮细胞不是被这些寄生虫感染,”他说。
进一步探索









用户评论