研究表明,癌症消瘦的部分原因是肿瘤因素阻碍了肌肉修复
一项新的研究表明,肿瘤向血液中释放抑制受损肌肉纤维修复的因子,这导致了癌症消瘦期间的肌肉损失。这种情况也被称为癌症恶病质,伴随某些类型的癌症,会导致危及生命的体重和瘦肌肉量的下降,并且是高达四分之一的癌症死亡的原因。这种情况没有治疗方法。
这项研究是由俄亥俄州立大学综合癌症中心-亚瑟·g·詹姆斯癌症医院和理查德·j·索罗夫研究所(OSUCCC - James)的研究人员领导的,它指出了新的治疗策略和新的药物靶点癌症恶病质。
研究结果发表在临床研究杂志.
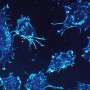
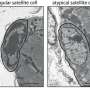
研究人员观察了肌肉干细胞,也被称为卫星细胞。这些细胞与肌肉纤维它们是修复受损纤维的必要物质。正常情况下,肌肉纤维的损伤会导致这些干细胞增殖并分化成成熟细胞肌肉细胞.这些肌肉细胞然后与周围受损的纤维融合,以限制肌肉萎缩。研究人员说,这一过程在癌症恶病质期间被阻断。
“我们的研究表明,尽管肌肉干细胞在恶病质期间被激活,但肿瘤释放的因子阻止这些细胞分化为肌肉细胞,这使得它们无法修复恶病质肌纤维,”首席研究员Denis Guttridge博士说,他是分子病毒学、免疫学和医学遗传学教授,也是OSUCCC - James分子生物学和癌症遗传学项目的成员。
“通过识别能够克服障碍并允许肌肉干细胞分化的药物,有可能恢复肌肉并提高患有恶病质的癌症患者的生活质量。”
在这项研究中,Guttridge和他的同事使用了动物模型和恶病质胰腺癌患者的组织,以确定肌肉微环境中导致癌症恶病质的因素。主要发现包括:
- 恶病质与肿瘤诱导的损伤有关骨骼肌细胞与肿瘤诱导的肌肉干细胞增殖
- 肌肉干细胞因子Pax7的过度表达,会阻碍细胞的分化能力,并促进癌症诱导的消瘦;
- Pax7的过表达通过阻断肌肉细胞的成熟及其与周围纤维的融合来促进癌症的消耗,从而使肌肉增加质量;
- Pax7的过表达由nf - κ B (NF-kB)控制,NF-kB已被证明在癌症中发挥多种作用。在恶病质中,NF-kB导致Pax7表达的紊乱,进而损害肌肉祖细胞的分化细胞并促进肌肉萎缩;
- 由于其组织特异性,Pax7抑制可能为癌症恶病质提供一种有吸引力的治疗方法。
“几十年来,恶病质的研究主要集中在骨骼肌纤维内导致肌肉萎缩的机制上,”Guttridge说。“我们的研究首次证明了肌肉纤维外和肌肉微环境内发生的事件也在推动癌症中的肌肉萎缩中发挥作用。”
进一步探索









用户评论