研究人员利用iPSC技术在体外建立家族淀粉样变性模型
来自波士顿大学医学院(BUSM)和波士顿医学中心(BMC)的研究人员从一名家族性转甲状腺素淀粉样变(ATTR)患者身上生成了首个已知的疾病特异性诱导多能干细胞(iPSC)系。研究结果发表在干细胞报告,可能会为家族性淀粉样变等遗传疾病带来新的治疗方法。
iPSCs是干细胞的一种形式细胞这些细胞来自皮肤或血液细胞,它们被重新编程成能够成为身体任何类型组织的细胞。ATTR是一种致命的常染色体显性蛋白质折叠障碍,由转甲状腺素(TTR)基因100多个不同突变之一引起。在ATTR中,肝脏分泌的蛋白质在目标器官(主要是心脏和周围神经系统)中聚集并形成原纤维,这突出了对能够复制这种临床可变疾病的多系统复杂性的模型的需求。
根据使用iPSC技术的研究人员的说法,可以建立与细胞来源的个体在遗传上完全相同的细胞系,从而允许在患者的个性化遗传背景下进行疾病建模和开发新的治疗方法。
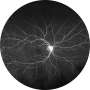
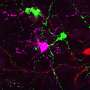
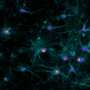
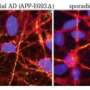
在这项研究中,研究人员使用iPSC产生分泌疾病特异性的肝细胞突变蛋白以及心脏和神经细胞即该病的下游靶组织。与暴露于正常蛋白质的细胞相比,暴露于突变蛋白质的心脏和神经元细胞显示出应激迹象,细胞死亡水平增加,从而在体外重现疾病的基本方面。此外,正在临床试验中测试的突变蛋白的小分子稳定剂在该模型中显示了有效性,验证了这种基于ipsc的患者特异性体外系统作为测试治疗策略的平台。
“我们的工作表明,使用来自患者的谱系指定细胞,在相对较短的时间内模拟复杂的多系统遗传疾病是可能的干细胞BUSM和BMC的血液学和肿瘤学医学助理教授、再生医学中心(CReM)联合主任George J. Murphy博士解释道。
“这是一项重大突破,将有助于测试针对ATTR开发的新型靶向疗法淀粉样变BUSM和BMC淀粉样变性中心的临床主任John Berk医学博士说,这些罕见疾病已经被研究了50多年。“来自世界各地来我们这里接受治疗的患者和家属可能很快就会从这项研究中受益。”