抑制支糖分子的形成可能导致新的治疗多发性硬化症
多发性硬化症是一种使人衰弱的疾病,涉及myelin-the脂肪组织的变性,使神经纤维,帮助他们进行冲动。这一过程,称为髓鞘脱失,会导致赤字的感觉、运动和思维过程,取决于哪些神经纤维的影响。取代了髓磷脂是一种很有前途的方法治疗多发性硬化及相关疾病,但机制脱髓鞘和remyelination仍然知之甚少。
在研究开辟了一个令人鼓舞的大道新疗法的发展,Naoyuki谷口和他的同事们从RIKEN-Max普朗克系统化学生物学联合研究中心的显示remyelination被糖分子被称为分支O-mannosyl聚糖。
谷口和他的同事们转基因的老鼠携带突变基因编码酶N-acetylglucosaminyltransferase-IX (GnT-IX)催化的分支O-mannosyl多糖糖蛋白质在大脑中。使用这些小鼠,研究人员发现,GnT-IX作用于一个特定的脑蛋白受体蛋白质酪氨酸磷酸酶吗?(RPTP ?),此前在脱髓鞘发挥至关重要的作用。
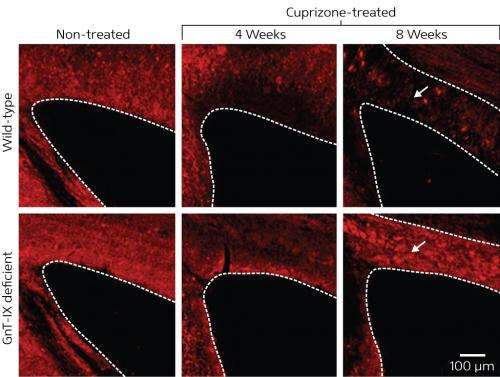
接下来,美联储研究团队正常和突变小鼠的饮食含有神经毒素cuprizone,通常引起脱髓鞘。在过去的八个星期,正常老鼠经历逐渐被发现髓鞘脱失的胼胝体——主要的白质束连接大脑的两个半球(图1)。相比之下,尽管在胼胝体髓鞘退化了四个星期的突变体,髓鞘形成明显增加了八周马克,这表明GnT-IX基因增强remyelination的缺陷。
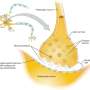
进一步的实验显示,cuprizone治疗可以激活non-neuronal以及星形胶质细胞进入一种疾病状态,导致他们表达RPTP ?包含分支O-mannosyl聚糖。在野生型小鼠,激活星形胶质细胞表达这些分支O-mannosyl多糖分子,抑制remyelination。在老鼠GnT-IX基因缺陷,然而,激活星形胶质细胞很少,没有支O-mannosyl聚糖允许髓细胞的分化和remyelination神经纤维在胼胝体。
“我们希望推出的分子机制支O-mannosyl多糖激活星形胶质细胞,”他说。“理解底层机制对开发一种药物治疗很重要多发性硬化症。"
球队未来计划GnT-IX抑制剂减弱星形胶质细胞激活屏幕。“困难的一件事是,药物通过血脑屏障,因此与临床医生合作将是重要的,”他指出。
更多信息:Kanekiyo, K。,等。失去支在星形胶质细胞加速remyelination O-mannosyl聚糖,《神经科学杂志》上33岁,10037 - 10047 (2013)。dx.doi.org/10.1523/jneurosci.3137 - 12.2013