重新定义Rett综合征基因功能障碍
怀特黑德研究所的研究人员重新定义了一个基因的功能,该基因的突变导致Rett综合征,一种神经发育性自闭症谱系障碍。这项新研究提供了对Rett综合征患者神经元缺陷的更好理解,并可能导致该疾病的新疗法。
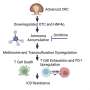
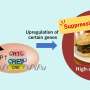
“MECP2的动作蛋白质与过去15年的举办方式正好相反,”怀特黑德的创始成员鲁道夫·杰尼施说,他也是麻省理工学院的生物学教授。“人们认为这种蛋白质可以全面抑制甲基化DNA的表达。这项工作表明,当你以一种考虑细胞大小的方式进行分析时——Rett的细胞大小非常不同神经元与野生型相比,我们突然发现这种蛋白质就像一个全局激活剂。我们用一种完全不同的方式定义了MECP2的功能。”
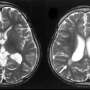
雷特综合征是一种与x有关的遗传疾病,每1万名新生女婴中就有1人患病。患有这种疾病的婴儿在最初的6到18个月发育正常,这时他们的运动和语言技能开始恶化。到四岁时,语言丧失、头变小、呼吸和心律不规则以及类似自闭症的症状是很常见的。有些症状可以用处方药治疗,但目前还没有治愈或改善疾病的疗法。Jaenisch实验室之前的工作为Rett患者的家庭带来了一些希望。在一个缺乏MECP2基因的小鼠模型中,注射了IGF-1蛋白的小鼠比未注射的小鼠呼吸和心律更规律。MECP2基因在约95%患有Rett综合征的女孩身上发生了突变。此外,治疗小鼠的大脑有更大的质量和更多的重要神经元投射,而这些在Rett综合征小鼠和人类患者中是缺失的。
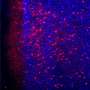
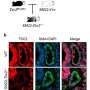
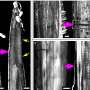
在目前的研究中,Jaenisch实验室的博士后研究员Yun Li分析了来自人类胚胎干细胞的mecp2缺陷神经元的整体基因表达。与之前的研究不同,李在比较它们时考虑到了Rett神经元较小的尺寸基因表达到MECP2完整的神经元。Rett神经元的mRNA转录减少蛋白质合成AKT/mTOR信号通路被IGF-1激活,存在严重缺陷。李的研究发表在10月2日的《美国医学杂志》上细胞干细胞.
“我们一直觉得很奇怪的是,MECP2突变小鼠和患有Rett综合征的孩子一样有许多严重的神经问题,但在微阵列上检测到的转录变化很少。这似乎并不支持MECP2蛋白的整体抑制作用。肯定是哪里出了问题。”“现在我们在细胞水平上对MECP2的功能和疾病的严重程度有了更好的了解。了解人类Rett神经元在整体转录和翻译方面的受损对我们设计Rett的治疗策略很重要。已知BDNF和IGF-1等生长因子可激活AKT/mTOR通路并增加蛋白质合成。未来,我们有兴趣进一步探索Akt/mTOR通路,并研究激活这一通路如何逆转疾病。”