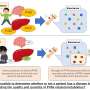
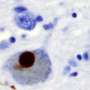
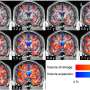
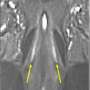
独特的蛋白质相互作用可能推动帕金森病的最常见的遗传原因
帕金森病的最具破坏性的方面可能不是它的衰弱症状,罗布其能力控制自己的运动的受害者。它可能不是世界上数百万和他们的家人每天遭受疾病的有害影响。相反,它可能,其根本原因在很大程度上仍是个谜。但是现在,斯顿研究院的科学家们发现两个蛋白质之间的相互作用在大脑中燃料类的退化和死亡的脑细胞,或神经元,导致帕金森氏症。这些发现,传统观念形成鲜明对比,为开发治疗奠定必要的基础,目标疾病的潜在机制。
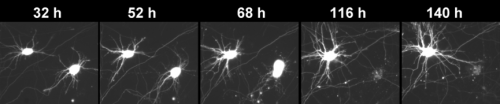
在最新一期的神经科学杂志》上网上,现在,科学家们在实验室里的格莱斯顿调查员史蒂夫·芬克贝涅医学博士,利用他们的力量独一无二的机器人显微镜跟踪单个神经元的寿命。显微镜已被用于研究各种各样的神经退行性疾病,在这项研究中,他们将注意力集中在LRRK2-the帕金森氏症的最常见的遗传原因。
科学家早已知道,体内基因LRRK2突变导致体内基因LRRK2错误折叠的蛋白质积聚在神经元。体内基因LRRK2的的假设都是错误折叠增加一种叫做激酶的酶的活性,这加剧了激酶活动是什么促使细胞死亡。科学家们还研究了体内基因LRRK2基因突变的事实往往聚集到所谓的包涵体(IB)作为另一个因素疾病的发展过程。
”结果,研究人员利用IB的存在和提高体内基因LRRK2激酶活动作为一个标尺来衡量的有害的影响,而不是直接体内基因LRRK2测量水平,”芬克贝涅博士解释谁是神经研究所副主任格莱斯顿教授以及加州大学旧金山,格莱斯顿的附属。“但我们相信这些都是细胞的主要动力死亡所以我们决定仔细看看细胞内发生了什么。”
当研究神经退行性疾病如帕金森症,是由神经元的退化和死亡,传统工具通常只允许研究人员跟踪神经元死亡在人口水平。但有请博士Finkbeiner革命显微镜使人员遵循成千上万个人的生命neurons-offering最清晰的视图,在细胞的生命周期事件中发挥作用在其死亡。
研究人员生成的神经元来自两个来源:转基因老鼠体内基因LRRK2基因突变,和人类神经元来自LRRK2-related帕金森患者的皮肤细胞。然后他们追踪这些细胞随着时间的推移,监测体内基因LRRK2基因突变的积累和积聚导致细胞死亡。
“有趣的是,我们发现无论是IB的还是激酶活性的细胞毒性导致神经元死亡的直接原因,,“盖亚Skibinski说格拉德斯通的工作人员研究科学家,博士论文的主要作者。“相反,细胞死亡的根本原因似乎是直接绑定扩散体内基因LRRK2基因突变的积累。”
但随着研究小组的视线更近的生活神经元,他们发现了有趣的东西:一个独特的体内基因LRRK2突变体之间的相互作用和α-突触核蛋白,另一个蛋白质,一直与帕金森病有关。体内基因LRRK2的研究表明,帕金森患者的突变往往显示异常积累的α-突触核蛋白。但直到现在,这两个蛋白质之间的关系的确切性质仍不清楚。
“重要的是,我们发现在老鼠和人类细胞模型,将α-突触核蛋白减少细胞死亡由体内基因LRRK2基因突变引起的,”Skibinski博士继续说。“当我们近距离观察时,我们发现,α-突触核蛋白的损失导致体内基因LRRK2立即下降。”
研究小组推测,在患者体内基因LRRK2基因突变,α-突触核蛋白的累积体内基因LRRK2清除阻碍了细胞的能力,导致它的积累。体内基因LRRK2的随着时间积累,变成了有毒的细胞,细胞死亡。
“发现两个蛋白质之间的协同关系长期扮演着某种角色帕金森是一个巨大的一步发展中药物攻击疾病的潜在机制,“有请博士Finkbeiner说。”我们继续解开体内基因LRRK2α-突触核蛋白和精确的功能关系,我们正在停止帕金森对大脑的冲击。”
进一步探索