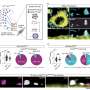
光遗传工具箱是多色的
光遗传学是一种技术,它允许科学家通过改造神经元来表达光敏蛋白,从而控制神经元的光电活动。在过去的十年里,它已经成为发现大脑中不同类型细胞功能的一个非常强大的工具。
这些被称为视蛋白的大部分光敏蛋白对蓝绿色范围的光有反应。现在,麻省理工学院领导的一个团队发现了一种视蛋白,它对红灯这使得研究人员可以同时独立控制两组神经元的活动,从而可以对神经元进行更复杂的研究大脑函数。
“如果你想了解两组不同的细胞是如何相互作用的,或者同一细胞的两个群体是如何相互竞争的,你需要能够独立地激活这些群体,”麻省理工学院生物工程、大脑和认知科学副教授、这项新研究的资深作者埃德·博伊登(Ed Boyden)说。
这种新的视蛋白是在120种藻类中发现的大约60种光敏蛋白之一。这项研究发表在2月9日的《美国医学杂志》网络版上自然方法,也产生了最快的视蛋白,使研究人员能够以毫秒的时间尺度精确研究神经元活动模式。
博伊登和阿尔伯塔大学医学和生物科学教授Gane Ka-Shu Wong是这篇论文的资深作者,第一作者是麻省理工学院博士后Nathan Klapoetke。来自霍华德休斯医学研究所珍妮利亚农场研究园区、宾夕法尼亚大学、科隆大学和北京基因组研究所的研究人员也对这项研究做出了贡献。
鲜活的色彩
视蛋白自然存在于许多藻类和细菌中,它们利用光敏蛋白来帮助它们对环境做出反应并产生能量。
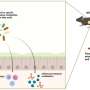
为了实现对神经元的光学控制,科学家们改造了脑细胞,使其表达视蛋白基因,这种视蛋白通过细胞膜运输离子来改变细胞电压。根据所使用的视蛋白,照射细胞可以降低电压并抑制神经元放电,也可以提高电压并刺激细胞产生电脉冲。这种效果几乎是瞬间的,而且很容易逆转。
使用这种方法,研究人员可以选择性地打开或关闭一群细胞,并观察大脑中发生了什么。然而,到目前为止,它们一次只能激活一个群体,因为唯一对红光有反应的视蛋白也对蓝光有反应,所以它们不能与其他视蛋白配对来控制两个不同的细胞群体。
为了寻找更多有用的视蛋白,麻省理工学院的研究人员与阿尔伯塔大学的Wong团队合作,后者正在对包括一些藻类在内的1000种植物的转录组进行测序。(转录组与基因组相似,但只包括细胞表达的基因,而不是其遗传物质的全部。)
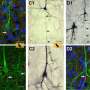
一旦研究小组获得了似乎编码视蛋白的基因序列,克拉珀特克就与麻省理工学院大脑、认知科学和生物学教授、麦戈文研究所(McGovern Institute)成员、论文作者玛莎·康斯坦丁-帕顿(Martha Constantine-Paton)合作,测试了它们在哺乳动物脑组织中的光反应性。研究人员将这种红光敏感视蛋白命名为克里姆森(crimson),它可以介导对735纳米波长的光作出反应的神经活动。
研究人员还发现了一种由蓝光驱动的视蛋白,它有两个非常理想的特征:它能高速工作,对非常微弱的光线敏感。这种视蛋白被称为克罗诺斯(Chronos),可以被弱到无法激活克丽姆森的蓝光刺激。
麻省理工学院媒体实验室和麦戈文大脑研究所的博伊登说:“你可以用短脉冲微弱的蓝光来驱动蓝色的,你可以用强红光来驱动克里姆森,这样你就可以在完整的脑组织中进行真正的双色零交叉信号激活。”
研究人员此前曾试图修改自然产生的视蛋白,使其反应更快,对较暗的光线做出反应,但试图优化一个特征往往会使其他特征变得更糟。
克拉波特克说:“很明显,当试图设计颜色、光敏感性和动力学等特性时,总会有权衡。”“我们非常幸运,某种天然物质的速度实际上比其他任何东西快几倍,光敏性也比其他任何东西高五到六倍。”
选择性控制
博伊登说,这些新的视蛋白有助于以前不可能的几种类型的研究。首先,科学家不仅可以操纵感兴趣的细胞群的活动,还可以控制上游细胞,通过分泌神经递质来影响目标细胞群。
克里斯姆森和克罗诺斯的配对还可以让科学家研究大脑内同一微电路中不同类型细胞的功能。这些细胞通常非常靠近,但有了新的视蛋白,它们可以被两种不同颜色的光独立控制。
到目前为止,大多数光遗传学研究都是在小鼠身上进行的,但克里姆森可以用于光遗传学研究果蝇,一种常用的实验生物。研究人员在果蝇身上使用蓝光敏感视蛋白时遇到了困难,因为光线会进入果蝇的眼睛并惊吓它们,干扰正在研究的行为。
Janelia农场的研究小组负责人、这篇论文的作者之一Vivek Jayaraman能够证明,当用红光刺激果蝇的克丽姆森时,这种惊吓反应不会发生。
因为红光对组织的伤害比蓝色的光博伊登说,在美国,克里姆森还具有最终用于人类治疗的潜力。用其他视蛋白进行的动物实验显示,在视网膜感光细胞丧失后,有希望帮助恢复视力。
研究人员现在正试图修改克丽姆森,使其对红外范围内的光线做出反应。他们也在努力使克里斯森和克罗诺斯更快,更多光敏感。
进一步探索