Anti-dsDNA, surface-expressed TLR4和endosomal TLR9识别合作加剧狼疮
系统性红斑狼疮(SLE)是一个复杂的多因子的自身免疫性疾病受许多基因和环境因素的影响。系统性红斑狼疮(SLE)的特点是高水平的anti-double-stranded DNA的存在自身抗体(anti-dsDNA)血清。此外,更大的系统性红斑狼疮患者中发现感染率和发病率和死亡率较高通常来自细菌感染。破译易感基因和环境因素之间的相互作用对红斑狼疮复杂的特征是具有挑战性的,导致了有限的成功。
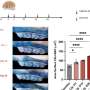
在6月出版的实验生物学和医学李等人,在台湾国立阳明大学,研究anti-double链DNA的作用(anti-dsDNA)和toll样受体(通常),TLR4和TLR9识别,红斑狼疮的发病机制。他们带着anti-dsDNA准备转基因小鼠转基因和挑战这些老鼠TLR4和TLR9识别受体激动剂。他们在anti-dsDNA证明转基因老鼠TLR4和TLR9识别合作与狼疮发展有关。
“既然同时激活的细胞外和细胞内的模式识别受体(PRR)能够引发更强烈的宿主免疫反应,这真的是关键的细胞外和细胞内确定co-engagement PRRs可能会增加疾病严重度狼疮,”博士说Kuang-Hui太阳,通讯作者。然而,只有个别条件基因敲除模型用于先前的研究研究TLR4的角色或TLR9识别。此外,细胞内核酸酸感性TLR9识别起到刺激或保护作用在不同的狼疮小鼠模型。因此,太阳和他的同事们TLR4的配体和TLR9识别注入anti-dsDNA转基因小鼠模型作为一种新的调查是否anti-dsDNA co-activation细胞外TLR4和endosomal TLR9识别影响的发病机制红斑狼疮在正常小鼠背景。他们的数据表明,除了anti-dsDNA,同时引发的信号通路激活surface-expressed TLR4和endosomal TLR9识别可以促进系统性红斑狼疮的进展。这些结果表明,同时针对anti-dsDNA, TLR4和9可能是一个潜在的治疗系统性红斑狼疮。
史蒂芬·r·古德曼博士主编实验生物学和医学说,“这些研究转基因小鼠为影响免疫耐受提供新的概念和降低系统性红斑狼疮疾病进展为开发未来疗法”。