神经细胞毒性蛋白的压力:生物标记神经元中确定和目标蛋白质脆弱
帕金森病是第二个最常见的神经退行性疾病。仅在德国,近一百万人受到影响。疾病的重点是中产生多巴胺的神经细胞的进行性变性在一定地区的中脑,黑质。错误折叠蛋白质的原因。直到最近,人们还不清楚为什么损害仅限于特定的神经细胞。或一个研究小组由法兰克福神经已经定义如何选择性疾病过程开始利用遗传帕金森小鼠模型;疾病。
某种类型的的进步的死亡神经细胞——多巴胺神经元-原因在黑质多巴胺缺乏的主要原因是电动机赤字在帕金森病人。虽然可以治疗一段时间多巴胺不足赔偿,如政府的左旋多巴和多巴胺受体激动剂,这些疗法并没有停止进步神经元的死亡。
在过去的二十年里,科学家们已经确定了基因突变导致神经退化和有毒蛋白质聚合体,与蛋白质a-synuclein有至关重要的作用。直到最近,人们还不清楚为什么只有特定类型的神经细胞,如dopaninergic黑质神经元,影响这一过程,而其他人,也表达突变a-syncuclein如多巴胺神经元附近,生存与小损伤的疾病进程。
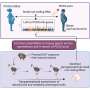
Mahalakshmi Subramaniam博士和教授领导的研究小组Jochen鲁普在歌德大学神经生理学研究所合作研究人员从法兰克福的实验性神经病学组和弗莱堡大学,首次证明了敏感的多巴胺黑质神经元功能如何应对有毒蛋白基因的小鼠模型。a-synculein突变基因(A53T),导致帕金森病在人类,小鼠模型的表达。
在最新一期的《神经科学杂志》上,研究人员报告说,敏感的多巴胺黑质神经元响应的积累有毒蛋白通过显著增加电动受灾中脑区域的活动。相比之下,越敏感,邻近的多巴胺能神经元并不影响他们的活动。”这个过程开始早在一年之前第一个赤字出现在多巴胺系统,因此提出了一种功能早期生物标志物可能未来潜力即将帕金森病的临床前检测人类,”亨·鲁普教授解释道。“潜在的早期临床前检测受试者的风险对神经保护治疗的发展至关重要。”
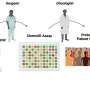
法兰克福,还发现了一个监管蛋白质,增加离子通道,使神经细胞电活动和相关的压力应对氧化损伤。这个频道提供了一个直接的多巴胺能神经元的神经保护的新靶蛋白。脑片,这种离子通道的功能作为一个“电动刹车”多巴胺神经元通过添加氧化还原可逆只是缓冲区。如果治疗药物能减少通道´s氧化还原敏感性在未来的小鼠模型,死亡的多巴胺神经元在黑质可能是预防。目前,研究人员正在研究是否与其他帕金森基因和类似的过程发生在衰老本身。“长期目标是调查这些结果在多大程度上从老鼠可能会转移到人类,”鲁普说。