细菌和免疫细胞打造一个富有成效的伙伴关系
为了防止感染,肠壁依赖于支持自己的“本土”的共生的细菌。这些肠道微生物群与和合作是反过来由宿主的免疫系统通过多种机制。作为一个研究小组由东京大学的博史清野第三坂本,Yoshiyuki Goto和他的同事们从理研生物资源中心已帮助照亮一个机制肠道微生物群和免疫细胞合作。
人口的研究始于发现肠道粘膜的上皮细胞,成为装饰着糖海藻糖。”之前的报告表明,上皮海藻糖对host-microbiota交互至关重要,“Sakamoto说。“这些数据促使我们识别机制,诱导上皮fucosylation。”
迄今为止的证据表明,与特定的交互共生的细菌刺激这种fucosylation直接。研究人员证实,老鼠完全缺乏肠道微生物群有更少的fucosylated上皮细胞,尤其是微生物的子集称为分段丝状细菌(SFB)出现这个过程作出重大贡献。然而,证期局不能实现这个fucosylation自己。研究小组发现,这些细菌必须合作免疫细胞称为类型3先天淋巴细胞(ILC3s)作为一线防御感染。
研究人员随后决定,与SFB互动和某些其他共生的物种造成ILC3s释放一个信号因子,刺激上皮负责fucosylation酶的生产。有趣的是,他们还发现,microbiota-independent分子由ILC3s功能协同诱导上皮fucosylation microbiota-dependent信号的因素。
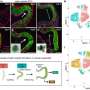
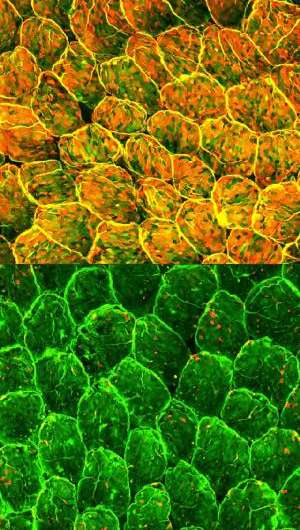
在一起,这些过程有助于形成一层海藻糖在肠道上皮细胞的表面,有效地防止感染。ILC3s引起的小鼠缺乏主fucosylation酶抑制fucosylation显示(图1)和被证明是更容易受到严重的感染鼠伤寒沙门氏菌,可能是因为致病细菌更容易附着在暴露肠道粘膜。
这些发现可能与多种疾病有关,和坂本打算在将来的研究中探索这种可能性。“这将是重要的识别识别上皮岩藻糖和如何将这些特定的细菌细菌影响等疾病的发展炎症性肠病,”他说。“更重要的是,它也将成为重要的检查机制我们这里显示是否直接适用于人类。”
更多信息:Goto, Y。Obata, T。Kunisawa, J。佐藤,S。伊万诺夫,即我。Lamichhane,。Takeyama, N。,Kamioka M。坂本,M。Matsuki, t . et al .先天淋巴细胞调节肠上皮细胞糖基化。科学345,1254009 (2014)。DOI: 10.1126 / science.1254009