越来越多的证据表明炎症是莱姆病神经系统表现的来源
约15%的莱姆病患者出现周围和中枢神经系统受累,常常伴有虚弱和疼痛的症状。发表在《莱姆病》杂志上的一项研究表明,炎症在一系列与莱姆病相关的神经系统变化中起着因果作用美国病理学杂志.杜兰国家灵长类动物研究中心和路易斯安那州立大学健康科学中心的研究人员还表明,消炎药地塞米松可以防止许多此类反应。
“这些结果表明,炎症在急性莱姆病神经螺旋体病的发病机制中起着因果作用,”Mario T. Philipp博士解释道,他是杜兰国家灵长类动物研究中心(Covington, LA)微生物学和免疫学教授、细菌学和寄生虫学系主任。
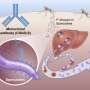
人类莱姆病是由感染螺旋体的蜱虫叮咬引起的包柔氏螺旋体burgdorferi(Bb)。Bb在全身扩散时,可引起关节炎、心肌炎和神经功能障碍。当涉及神经系统时,它被称为莱姆病神经螺旋体病(LNB)。外周神经系统LNB的临床症状可能包括面神经麻痹、神经源性疼痛沿背部辐射到腿和脚、肢体疼痛、感觉丧失或肌肉无力。中枢神经系统受累可表现为头痛、疲劳、记忆丧失、学习障碍、抑郁、脑膜炎和脑病。
为了进一步了解Bb感染的神经病理影响,研究人员对12只恒河猴进行了活体感染b . burgdorferi;两只未受感染的动物作为对照。在12只接种bb的动物中,4只接受了抗炎类固醇地塞米松治疗,4只接受了非甾体抗炎药(NSAID)美洛昔康治疗,4只仍未接受治疗。每组一半接种后研究8周,另一半接种后研究14周。
研究人员检查了炎症在bb感染动物神经系统中的作用。在所有感染动物的脑脊液中,炎症介质白细胞介素-6 (IL-6)、IL-8、CCL2和CXCL13的水平显著升高,以及白细胞增多(细胞计数增加,主要是白细胞)——使用地塞米松治疗的动物除外。“趋化因子如IL-8和CCL2已知可介导细菌性脑膜炎期间中枢神经系统隔室中免疫细胞的涌入,而CXCL13是神经炎症期间B细胞募集到脑脊液的主要决定因素,”Philipp博士解释道。
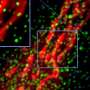
Bb感染导致未接受地塞米松治疗的感染动物出现许多组织病理学发现,如轻脑膜炎、血管炎、脑和脊髓局灶性炎症,以及颈脊髓坏死性局灶性神经退行性变和脱髓鞘。对背根神经节的评估显示,除地塞米松治疗的动物外,所有感染动物均出现炎症伴神经退行性变,以及神经元和卫星胶质细胞(包围感觉神经元)的显著凋亡。研究人员能够量化地塞米松治疗在保护卫星胶质细胞和神经元凋亡方面的保护作用;相比之下,美洛昔康治疗仅对卫星胶质细胞凋亡有保护作用,且只有在长时间给药后才有效。
感染活Bb(未用地塞米松治疗)的动物背根显示大量淋巴细胞和单核细胞的存在。有趣的是,注射部位附近的反应在组织学上与沿脊髓发现的弥漫性炎症不同。在背根神经节和感觉神经中发现的病理可以解释莱姆病患者在蜱虫叮咬起源附近所经历的局部疼痛和运动障碍。
一些莱姆病患者还表现出脱髓鞘神经病变和神经传导减慢的迹象。猕猴运动神经和感觉神经的神经传导研究表明,Bb感染导致特定的电生理异常(F波潜伏期和时间弥散增加),这可以通过地塞米松预防。
虽然抗生素是莱姆病的标准和必要的一线治疗,但结果显示抗炎或免疫调节剂对莱姆病相关神经螺旋体病具有潜在的治疗作用。Bb感染引起的大部分神经病理改变可通过广谱甾体抗炎药地塞米松预防,而非甾体抗炎药美洛昔康一般无效或仅部分有效。分析两种药物在作用机制上的差异,可能为LNB新辅助治疗的发展提供蓝图。
“重要的是,我们发现坏死性脊髓炎和变性脊髓,背根神经节神经退行性变,神经根脱髓鞘仅当淋巴细胞炎症病变时也观察到中枢神经系统和末梢神经系统,”菲利普博士说。“我们的结果表明,持续的细胞因子激活神经系统会导致疲劳、疼痛和认知功能障碍等持续症状,尽管患者曾接受过莱姆病治疗,但有时会出现这些症状。”