研究小组发现与造血干细胞有关的新基因
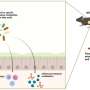
由密歇根大学生命科学研究所领导的研究已经确定了一个基因,该基因对控制人体从造血干细胞(即造血干细胞)中产生血细胞和免疫细胞的能力至关重要。
该研究结果将于临床研究杂志4月13日的一项研究为人体如何创造和维持健康的血液供应和免疫系统的基本机制提供了新的见解,无论是在正常情况下,还是在压力情况下,比如身体经历了一次中风骨髓移植。
除了帮助科学家更好地理解人体的基本过程外,这一发现还为Ash1l基因在已知涉及同一基因家族其他成员的癌症(如白血病)或Ash1l可能高表达或突变的癌症中的潜在作用开辟了新的探索方向。
该研究的资深作者伊凡·美拉德(Ivan Maillard)说:“如果我们想在出现问题时开发干预措施,了解健康个体的基本机制是如何运作的,这是至关重要的。”伊万·美拉德是生命科学研究所的副教授,也是他实验室所在的地方,也是密歇根大学医学院血液学-肿瘤学部门的副教授。
“白血病是人体造血组织的一种癌症,所以它显然是我们下一步计划研究的地方。如果我们发现Ash1l起作用,那么这将为试图从药理学上阻断或减缓其活性开辟途径。”
研究生摩根·琼斯和詹妮弗·蔡斯是这项研究的第一作者。
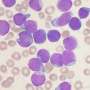
造血干细胞的功能障碍在白血病和骨髓衰竭等疾病中是众所周知的。用于治疗癌症的高剂量化疗和放疗也会破坏造血干细胞。这些细胞的替换通过骨髓移植是唯一在人类患者中广泛建立的涉及干细胞的疗法。
但即使没有疾病,血细胞需要不断地更换——大多数血细胞的寿命从几天到几个月不等,这取决于它们的类型。
在五年多的时间里,Maillard和他的合作者发现了Ash1l基因在调节这些造血干细胞的维持和自我更新潜力方面所起的一个以前未知但基本的作用。
Ash1l(缺失的,小的或同源的1-like)基因是一个基因家族的一部分,该基因家族包括MLL1(混合谱系白血病1),一个在患有白血病的患者中经常突变的基因。研究发现,这两种基因都有助于血液更新;在缺少其中一种的小鼠中可以看到轻微的缺陷,但缺少两者会导致灾难性的缺陷。
美拉德说:“我们现在有明确的证据表明,这些基因合作可以形成健康的血液系统。”
他的实验室对该基因的调查开始于合著者莎莉·坎珀的推动,莎莉·坎珀是詹姆斯·v·尼尔教授,密歇根大学医学院人类遗传学系主任。坎珀一直在研究Ash1l在内分泌和生殖器官中的作用,并发现了造血组织也可能受到影响的线索。
研究发现:
ash1l缺陷小鼠有正常数量的造血干细胞在发育早期,但成熟时缺乏干细胞,这表明细胞不能在骨髓中适当地维持自己。
ash1l缺陷干细胞在骨髓移植后无法建立正常的血液更新。此外,ash1l缺陷干细胞在骨髓中与正常造血干细胞竞争不足,很容易被移位。
Ash1l调节多个下游“同源异型”基因的表达,这有助于确保发育中的生物体的正确解剖结构。
美拉德说:“这一研究领域真正展示了我们从人类患者身上学到的知识与在实验室环境中进行的发现之间的动态相互作用。”
美国在广岛和长崎投下原子弹后,医生们注意到,受辐射的患者无法产生新的细胞白细胞防止感染。随后在老鼠身上的实验证明了这一点骨髓将健康的动物移植到受过辐射的动物体内可以恢复它们制造新血细胞的能力。这项技术最终被开发用于人类患者,包括那些血液干细胞都被癌症治疗杀死了。但在实验室环境下工作仍在继续。
“通过继续研究基本的、潜在的机制——建立在果蝇和小鼠的研究历史上——我们正在帮助解开血液更新的复杂机制,这可能为5年、10年或20年后的新的人类治疗奠定基础,”Maillard说。
进一步探索