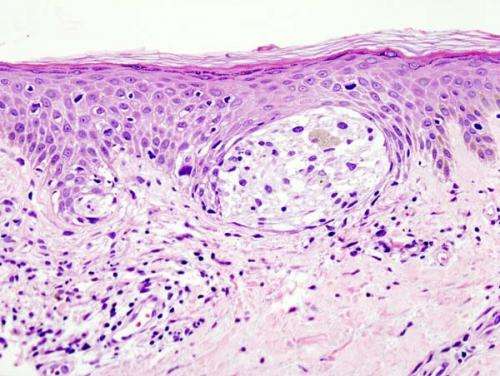
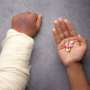
黑色素瘤在皮肤活检)为这情况可能是肤浅的黑色素瘤扩散。来源:维基百科/ CC冲锋队3.0
靶向治疗的发展大大改善了黑色素瘤患者的生存在过去的十年里;然而,病人经常复发,因为许多疗法不杀死所有的肿瘤细胞,剩下的细胞适应治疗和产生耐药性。莫菲特癌症中心研究人员发现一种新的机制,导致黑色素瘤细胞对药物的抗药性,目标蛋白质BRAF。
BRAF基因突变是最常见的突变中发现黑色素瘤,高达50%的肿瘤检测呈阳性的突变。几个代理,直接目标BRAF已经被美国食品和药物管理局批准用于治疗黑色素瘤患者的突变,包括dabrafenib和vemurafenib。然而,许多患者产生耐药性BRAF抑制剂和复发。这种阻力与激活BRAF蛋白的沟通途径肿瘤细胞。
另一个经常基因突变的PTEN在黑色素瘤。研究表明,黑色素瘤患者都有BRAF和PTEN突变可能贫穷回应dabrafenib和vemurafenib治疗。
莫菲特研究人员想要确定机制负责抵抗BRAF抑制剂。他们发现BRAF抑制剂导致BRAF和PTEN突变黑色素瘤细胞增加纤连蛋白的水平。纤连蛋白是一种蛋白质,它是表达在细胞周围的空间。研究人员发现,高水平的纤连蛋白使黑色素瘤细胞形成自己的保护环境,减少了BRAF抑制剂杀死肿瘤细胞的能力。
重要的是,研究人员发现,黑素瘤患者PTEN突变更高的水平纤连蛋白的肿瘤往往有较低的总生存期。他们还表明,针对肿瘤BRAF抑制剂结合的药物目标保护环境显著增强杀死BRAF抑制剂的影响。
“这项研究提供了重要的新见解为什么几乎所有黑色素瘤患者靶向治疗失败,”解释Keiran斯莫利,博士,副莫菲特肿瘤生物学项目的成员。
研究人员认为,在未来有效的癌症治疗需要药物的联合行动的目标肿瘤初始治疗和它的适应性反应。这对于黑色素瘤患者尤其重要,因为只有一个细胞的生存初始癌症治疗后足以允许黑色素瘤肿瘤再生。根据Inna Fedorenko博士,博士后研究员莫菲特,”目标提供更持久的保护环境是一种治疗对患者的反应。”
该研究发表之前6月15日在线打印杂志上致癌基因。
更多信息:纤连蛋白诱导废除的BRAF抑制剂反应BRAF V600E / PTEN-null黑色素瘤细胞,致癌基因提前在线出版2015年6月15日;DOI: 10.1038 / onc.2015.188
期刊信息:致癌基因
所提供的h·李·莫菲特癌症中心和研究所