杂交细胞会引起癌症周围的混乱
莱斯大学的研究人员已经建立了一个模拟,以显示癌症肿瘤如何为了自己的利益而操纵血管生长。
像所有细胞一样,肿瘤细胞需要进入人体精细的血管网络,为它们带来氧气并带走废物。肿瘤已经学会了利用所谓的血管生成过程,在这个过程中,新的血管从现有的血管中发芽,就像树枝从树上长出来一样。
但一些细节直到现在才被隐藏起来。
通过抗血管生成阻止肿瘤的能力是癌症治疗的目标之一。莱斯大学理论生物物理中心的科学家们的这项新工作将帮助研究人员用复杂的计算机模型快速测试策略。
由莱斯大学理论物理学家José Onuchic和Eshel Ben-Jacob领导的团队创建了一个详细的模型,描述了参与血管生成的蛋白质如何相互通信,以及肿瘤如何控制控制血管生长的蛋白质信号链。
这项研究的一个关键发现在本周的美国国家科学院院刊表明被称为“锯齿状”的配体在混沌中起着主要作用船的增长观察肿瘤周围。
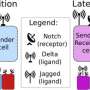
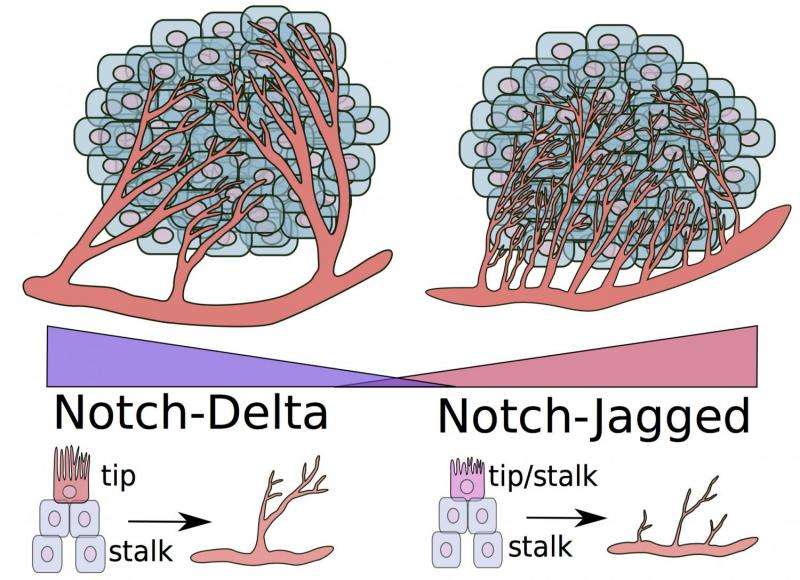
在正常的生长过程中,内皮细胞从现有的血管顶端生长出来,而其他沿着顶端细胞生长的细胞成为柄细胞,最终形成血管壁。细胞间notch信号通路指导内皮细胞决定成为尖端或柄。
Notch受体是与细胞产生的δ配体或锯齿配体分子结合的蛋白质。它们相互作用的方式决定了细胞的命运。当缺口和δ结合时,它们促使一些细胞成为尖,相邻的细胞成为柄;这是如何发生的,这是莱斯大学早期研究的主题。
但是锯齿状配体的作用已经出现在新的模型中。因为jagged在肿瘤在环境中,锯齿状缺口结合压制了三角缺口结合,产生了一种新的细胞,尖柄杂交细胞。虽然这些细胞仍然可以形成新的血管,但这些血管很少成熟。
该论文的合著者、莱斯大学生物工程研究生莫希特·库马尔·乔利(Mohit Kumar Jolly)说:“血管会发出许多分支,但很少有分支像正常血管生成过程中那样发育良好。”
“高水平的锯齿在环境中可以触发形成血管主要作者Marcelo Boareto补充道,他曾是莱斯大学的访问学者,现在是苏黎世瑞士联邦理工学院的博士后。
“肿瘤不需要等待血管发育,”奥努奇克说。“他们利用了建筑结构的漏洞。”
据研究人员称,notch-delta途径已经被大量研究,并且是目前使用的许多抗血管生成药物的靶点。Boareto说:“我们想知道,到底有什么notch-锯齿信号在notch-delta信号中没有做到。”“我们发现,当细胞主要通过锯齿状进行交流时,我们看到了一种新的细胞,它既不是尖端,也不是柄,而是介于两者之间。
他说:“这种受损细胞是正常血管生成和肿瘤血管生成之间的主要区别,这表明如果notch-jagged信号可以在不影响notch-delta的情况下以某种方式被抑制,我们可能会破坏肿瘤血管生成。”
Onuchic说,目前大多数抗血管生成疗法都是针对整个notch信号。“这种药有很多副作用,而且不能特别治疗糖尿病肿瘤血管生成他说。
他指出,该模型还考虑了血管内皮生长因子(VEGF)的影响,VEGF是一种引发血管生成的蛋白质,并在肿瘤中过表达细胞.“非常有趣的是,肿瘤如何劫持这一重要的机制,这是功能性血管发育所必需的,并将其放大以产生病理病变血管生成这导致了不受控制的增长。”
更多信息:Jagged通过影响尖柄命运决定来调节正常和肿瘤血管生成的差异,Marcelo Boareto,DOI: 10.1073 / pnas.1511814112