实验抗癌药物显示了多发性硬化症的治疗在小鼠模型的承诺

一种实验性药物最初确定的国家癌症研究所图书馆化合物作为一个潜在的治疗大脑和基底细胞癌的症状改善小鼠的神经系统衰弱疾病多发性硬化症(MS),根据纽约大学Langone医学中心的一项新的研究。
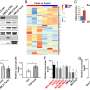
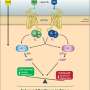
实验药物受雇于纽约大学Langone的神经科学家叫做GANT61团队。它阻碍了行动的一个关键的蛋白质,Gli1,参与所谓的声波刺猬信号、生物通路密切相关神经干细胞发展和某些癌症的增长,是谁的信号在组织样本取自脑损伤患者的女士。
一份报告描述研究结果被发表在《华尔街日报》自然在线9月30日。
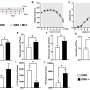
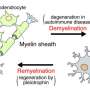
在这项研究中,老鼠与大脑化学破坏髓鞘有每日剂量的GANT61一个月。结果表明,小鼠接受药物有髓治疗结束时多50%比未经处理的老鼠。髓磷脂是nerve-protecting鞘的退化是一个女士的主要原因。
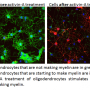
此外,研究人员说,他们发现GANT61-treated小鼠神经的数量增加了8倍干细胞迁移到myelin-damaged的大脑区域,并最终发展成myelin-producing少突胶质细胞。未经处理的小鼠没有增加。
临床,研究人员报告,药物治疗小鼠能够恢复从最初一轮MS-like瘫痪和腿的弱点。未经处理的老鼠然而,经历了反复的发作的腿和膀胱的弱点,症状类似经历的人。
据研究高级研究员詹姆斯·沙尔茨医学博士的实验,历时六年完成,被认为是第一个证明神经干细胞,而不只是oligodendrocytic细胞的早期形式,可以被修改,加入了髓鞘修复。目前的治疗目标免疫系统主要是缓慢的疾病,主要目标在大脑和脊髓髓鞘,但临床专家尚未能够修复伤痕累累,髓鞘退化。
沙尔茨,纽约大学Langone教授及其海伦和马丁Kimmel干细胞生物学中心和Druckenmiller神经科学研究所说,研究小组的最新发现也第一个表明药物针对声波刺猬,通路在1980年代首次发现,可以治疗神经系统疾病,如女士。
团队的最新研究,他说,也是第一个强有力的证据多发性硬化症针对声波刺猬通路的一部分有完全不同的效果比整个通路阻塞,在其他实验其他地方没有产生任何remyelination而是停止少突细胞成熟。
“我们的研究结果表明,治疗多发性硬化的一个潜在的长期战略将涉及单独治疗目标神经干细胞,帮助把它们变成成熟的少突胶质细胞,以及年轻的和不成熟的少突胶质细胞产生更多的髓鞘,“沙尔茨说。
“我们的发现也明确表示,有一个常住人口的成年神经干细胞可以治疗目标和招募的障碍,”沙尔茨说。
领导研究调查员Jayshree Samanta,面交博士说,研究小组计划进一步的实验,随着社会国家多发性硬化症的专项资金,开发一个更好的Gli1抑制剂药物,沙尔茨,Samanta, Fishell,纽约大学已获得一项专利。
研究人员说,他们的最新发现和未来的项目确认纽约大学Langone致力于研究女士的根本原因和症状,以及开发治疗疾病。他们还说他们的基本研究支持女士和强调了护理工作的综合模型在纽约大学Langone多发性硬化症综合保健中心。
更多信息:抑制Gli1动员remyelination内源性神经干细胞,自然,DOI: 10.1038 / nature14957