另一种炎症
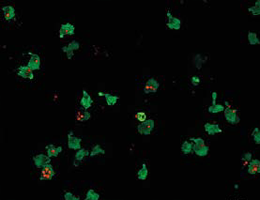
使用新开发的组合方法,研究Ludwig-Maximilians-Universitaet (LMU)在慕尼黑免疫学家Veit霍农定义了一个前所未知的途径,引发炎症。
脊椎动物的免疫系统能够区分“自我”和“非自我”组件,使识别和破坏入侵病原体和肿瘤细胞等异常的细胞类型。适应性免疫反应,如基于抗体,是强大的和非常具体的,但需要繁琐和耗时的基因重组。立即有效防守,必须迅速发现入侵者,这任务是由所谓的先天免疫系统。天生的免疫细胞表达一个相对较小的表面受体,它识别独特的分子结构与病原体有关。绑定这些结构引发炎症反应,杀死病原体或受感染的细胞。为了分析信号通路调节这些过程,研究Veit霍农,握着的椅子Immunobiochemistry LMU基因中心,结合两种不同的方法。他们首先利用一种新型细胞培养系统,模拟单核细胞的功能,一类免疫细胞参与调节炎症。然后他们系统地删除单个基因决定启动炎症反应的作用,发现了一个前所未知的信号途径。该发现发表在《华尔街日报》免疫力。
霍农教授和他的团队开始他们的研究的蛋白复合物称为NLRP3 inflammasome波恩大学医院2015年10月在他搬到LMU之前。这个复杂的存在于单核细胞,诱导炎症中扮演着重要角色,除了涉及疾病与慢性炎性反应有关,如痛风、2型糖尿病和动脉硬化。然而,我们的知识的作用方式主要是基于在老鼠的细胞进行研究。在小鼠单核细胞,需要两个刺激导致NLRP3 inflammasome引发炎性信号蛋白的分泌白介素- 1β(il - 1),而新鲜的孤立人类发现单核细胞产生il - 1在回应一个信号,它通过一种TLR4受体。但是,没有建立人类monocyte-like细胞系对这个信号作出反应。这就是为什么霍农和他的同事们雇佣了新的人类monocyte-like细胞系为了理解的物种差异的基础。
“我们专门开发了一个程序,允许我们删除单个基因在培养人类免疫细胞人类单核细胞相似。使用这个系统,我们可以确定,在基因水平,负责信号传输的组件,和激活的NLRP3 inflammasome,”莫里茨Gaidt解释说,博士生在霍农集团和这项新研究的第一作者。这样,团队能够分析il - 1的分泌由人类单核细胞以前所未有的细节,来定义机制,使人类NLRP3被激活在回应一个信号。
研究人员由暴露他们的单核细胞TLR4受体激活细菌脂多糖(LPS)——一个复杂的分子组成的糖和脂肪,这是许多病原菌表面发现。然后显示绑定的有限合伙人触发器的分泌il - 1通过一个以前从未发现过的信号继电器。“这个新通路的激活解释了为什么人类单核细胞分泌il - 1不需要第二个信号。相反,在小鼠单核细胞这一特定通路不激活,所以第二个刺激计划是必需的,”Veit霍农解释道。此外,尽管inflammasome激活鼠标诱发炎症细胞程序性死亡,人类单核细胞中不使用的途径。“我们将这个信号通路称为替代inflammasome,为了区别于之前描述的途径,“霍农说。“我们相信,这一信号通路发挥了至关重要的作用在人类炎症过程。”
新的研究结果突显出事实在老鼠对人类并不总是可翻译。到目前为止,只有人类单核细胞被发现反应直接接触有限合伙人通过释放白介素1,不需要第二个信号。研究者们现在打算分析已TLR4受体在其他生物模型的函数。使用霍农monocyte-like细胞,可以进一步确定信号通路体外。“我们的研究结果驳斥一些古典inflammasome研究的原则。我们希望我们的新方法还将加强我们的理解细胞的生物学基础免疫疾病,”霍农总结道。
更多信息:莫里茨m . Gaidt等。人类单核细胞接触另一种Inflammasome通路,免疫力(2016)。DOI: 10.1016 / j.immuni.2016.01.012