孕产妇细菌感染引发胎儿大脑神经元异常增殖
圣裘德儿童研究医院的科学家们已经发现的细菌细胞壁穿过胎盘,进入发展中神经元,胎儿出生后大脑解剖学和认知功能改变。今天的研究发表在《科学》杂志上细胞宿主和微生物。
结果在实验模型可能构成之间的关系提供了一个可能的机制孕产妇细菌感染在怀孕期间和孤独症的风险增加和其他儿童的认知问题。研究还提出了质疑这类的抗生素应该用于治疗感染。
“意料之外的发现,因为在儿童和成人肺炎球菌感染可导致脑膜炎和神经元的死亡,”说,该研究的通讯作者伊莱恩Tuomanen,医学博士圣裘德传染病部门的主席。“这项研究在细菌感染的小鼠模型发现,产前正好相反。证据显示产妇感染导致信号事件导致扩散重组的神经元在发育中的大脑缺陷在某种程度上,可能由于过度拥挤。”
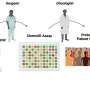
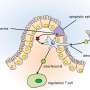
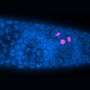
研究人员首次显示,部分细菌细胞壁穿过胎盘并前往胎儿大脑,导致未成熟神经元的增殖。证据表明,扩散是引发了一种以前未被认识的途径,包括先天免疫系统,调节基因表达的一种蛋白质。
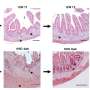
扩散导致神经元增加了50%在区域发展中大脑皮层,负责思想、行动和其他高级功能。
调查人员还报告说,老鼠在胎儿发育早期接触细菌细胞壁后表现低于平均记忆和认知功能的措施。研究人员发现证据表明抗生素氨苄青霉素治疗感染的孕产妇,破坏细菌和发送部分细胞壁进入血液,导致类似的神经元增加。
Tuomanen说结果质疑应该使用哪个类抗生素治疗细菌感染在怀孕期间。“这项研究表明广泛使用的抗生素如氨苄青霉素导致细菌细胞壁破裂,释放可能导致大脑发育的变化,”她说。“这种变化没有出现在小鼠与克林霉素等抗生素杀死没有释放细胞壁。
“还需要更多的研究来了解不同种类的抗生素的长期影响妊娠结局,“Tuomanen说。
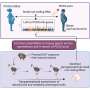
在细胞生长在实验室和在老鼠中,研究人员展示了作品的肺炎球菌细胞壁结合蛋白质血小板活化因子受体(PAFr)运输在胎盘进入胎儿的大脑。
在那里,而不是引发炎症和细胞死亡,数小时内细菌细胞壁FoxG1打开了表达的蛋白质。FoxG1是一个转录因子驱动神经扩散。扩散发生在怀孕早期深在大脑的一个区域称为心室区。几天之内,研究者记录皮层神经元板增加了50%,这成为了皮层。
研究人员还报告说,先天免疫系统的一个组成部分发挥了关键作用在推动扩散而不是炎症。蛋白质命名toll样受体2 (TLR2)帮助细胞识别和抵御细菌。来自本研究的证据表明,TLR2合作伙伴提供一个相关的蛋白质,TLR6,驱动扩散对细菌细胞壁的回应。
没有TLR2,不成熟的胎儿神经细胞没有扩散。研究者也报道,扩散不发生在胎儿的老鼠缺乏PAFr或者TLR2,表明两种蛋白质发挥作用在大脑中对细菌细胞壁的反应。
“还需要更多的研究来了解细菌的细胞壁信号诱导扩散通过这个新发现的路径链接与转录因子的先天免疫受体TLR2 FoxG1开车在胎儿神经细胞增殖,”Tuomanen说。“这相同的机制可能会导致新的策略来修复或替换神经元失去的疾病或伤害。”