脑部监护人去除垂死的神经元
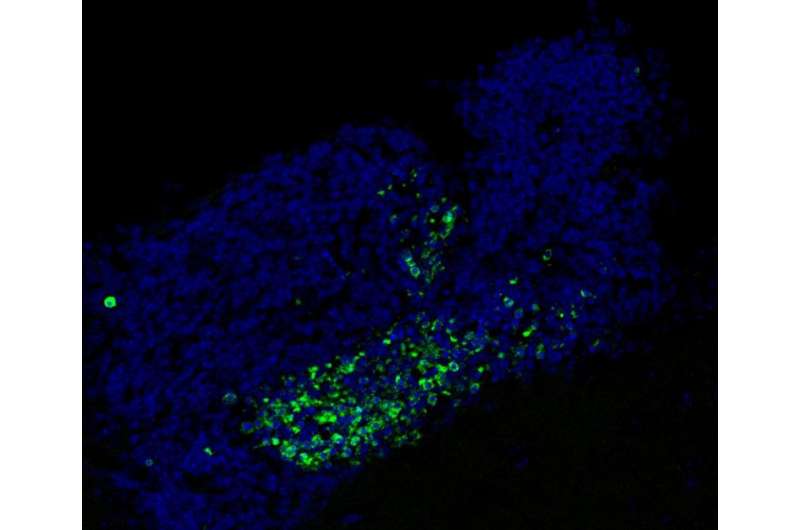
到青春期,您的大脑已经包含了您一生中您所拥有的大多数神经元。但是一些区域继续生长新的神经细胞,并需要细胞前哨的服务,即通过消除死亡或功能失调的细胞来确保大脑安全的专门免疫细胞。
现在,Salk科学家发现了垂死和死亡神经元被清除的令人惊讶的程度,并确定了这一过程关键的特定细胞开关。作品详细介绍了自然2016年4月6日。
“我们发现受体在免疫细胞在里面脑对健康和受伤状态都至关重要。与疾病有关,例如帕金森氏病。”
二十年前,Lemke Lab发现免疫细胞表达了称为TAM受体的关键分子,此后已成为许多实验室中自身免疫和癌症研究的重点。称为MER和AXL的两个TAM受体有助于称为巨噬细胞的免疫细胞充当垃圾收集器,识别和消费超过1000亿死细胞每天都会在人体中产生。
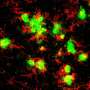
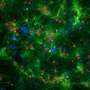
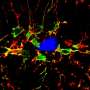
在当前的研究中,团队询问MER和AXL是否在大脑中完成了相同的工作。称为小胶质细胞的专门中枢神经系统巨噬细胞占大脑中约10%的细胞,它们在其中检测,反应和破坏病原体。研究人员在原本健康小鼠的小胶质细胞中删除了AXL和MER。令他们惊讶的是,他们发现缺乏两个受体会导致大量的死细胞堆积,但并非大脑中的任何地方。仅在观察到新神经元的产生(神经发生)的小区域中才能看到细胞尸体。
许多细胞在成人神经发生过程中正常死亡,但它们立即被小胶质细胞食用。“即使是正常大脑中的单个死细胞也很难,因为它们是如此有效地被小胶质细胞识别和清除,”论文和前Salk研究合伙人PaquiG.Través说。“但是在缺乏MER和AXL的小鼠的神经源区域中,我们发现了许多这样的细胞。”
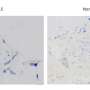
当研究人员通过标记小鼠缺失MER和AXL的新生长的神经元来更加仔细地检查了这一过程时,他们注意到了其他有趣的东西。迁移到嗅球或气味中心的新神经元在没有AXL和MER周围急剧增加。缺乏TAM受体的小鼠在嗅球中新产生的细胞比正常小鼠增加了70%。
根据莱姆克(Lemke)的说法,这种未经检查的新神经生长如何(在何种程度上)如何影响老鼠的嗅觉,尽管这是实验室将探索的领域。但是,更多的活神经细胞能够迁移到嗅球在没有受体的情况下,除清除死细胞外,MER和AXL还具有另一种作用 - 实际上,它们实际上可能靶向生命但在功能上受损的细胞。
Lemke说:“在神经源性区域中,细胞死亡的很大一部分不是由于细胞的内在死亡,而是小胶质细胞本身的结果,而小胶质细胞本身是由于吞噬而杀死了细胞的一小部分。”“换句话说,这些新生神经元的祖细胞中的一些实际上正在生存。”
Lemke补充说,这在健康大脑中不一定是一件坏事。大脑产生的神经元超过其所能使用的,然后将不需要的细胞修剪。但是,在发炎或患病的大脑中,生命的破坏细胞五月适得其反。
Lemke Lab进行了另外一系列的实验来了解TAM受体在疾病中的作用:他们研究了AXL和MER在帕金森氏病小鼠模型中的活性。该模型以遗传的疾病形式产生人类蛋白质,从而导致大脑变性缓慢。该小组认为,在这种情况下,AXL与其他研究相一致,表明增加AXL是组织炎症的可靠指标。
但是,当研究人员从帕金森氏症的老鼠中取出AXL和MER时,他们感到惊讶。与患有这种疾病的小鼠相比,与正常的小胶质细胞相比,丢失AXL和MER的小鼠实际上寿命更长。这可能是因为AXL和MER目标并破坏病人功能失调的神经元。在存在疾病的情况下,可能会出现功能失调的神经元,因此AXL和MER可能会促使太多神经元的破坏,实际上正在加快疾病。
“似乎我们可以通过操纵AXL和MER来修改动物模型中的疾病进程,”该论文和前Salk Research助理的联合第一作者Lawrence Fourgeaud说。该小组警告说,需要进行更多的研究来确定调节TAM受体是否可能是涉及小胶质细胞的神经退行性疾病的可行疗法。