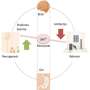
肠道菌群和大脑之间联系的新发现
肠道细菌可以增强勇气或引发多发性硬化症:越来越多的研究结果证实了“肠-脑轴”对神经病学的重要性,并表明许多神经疾病的触发因素可能位于消化道。
“肠道微生物组可以影响中枢神经系统、神经细胞的发育和免疫系统。更好地了解它的作用可能会彻底改变我们的治疗方案,”法国Jouy-en-Josas国家农学研究所的Patricia Lepage博士在哥本哈根举行的欧洲神经病学学会(EAN)第二届大会上指出。
肠道菌群影响行为
肠道微生物群是人体肠道微生物及其所有细菌、古菌、病毒和真菌的集合体。在很长一段时间里,认为微生物组也可以负责大脑外部的过程似乎很牵强消化道.然而,科学界不断发现更多惊人的细节。例如,最近对没有任何微生物(无菌)生长的实验室动物的研究表明,肠道中的微生物甚至能够影响行为。Lepage博士说:“肠道微生物可以产生对大脑有影响的神经介质。无菌小鼠比肠道内充满共生菌群的同类小鼠表现出更少的焦虑。然而,到目前为止,关于这一过程在人脑中如何运作的证据还很少。”
同时,肠道和大脑通过迷走神经、免疫系统、肠神经系统或微生物代谢过程等多种途径相互交流。例如,肠道细菌将碳水化合物转化为短链脂肪酸,如丁酸。这加强了细胞之间的联系,加强了血脑屏障,血脑屏障是保护大脑免受感染和炎症的细胞壁。
肠道微生物组调节大脑过程
对于神经科学家John F. Cryan教授(爱尔兰科克大学APC微生物组研究所)来说,毫无疑问,肠道微生物组调节着对神经疾病发展至关重要的基本大脑过程:“我们研究了无菌小鼠的大脑。在一个区域,前额叶皮层,我们发现与正常条件下的动物相比,有髓鞘形成增加。这可能对髓磷脂相关疾病有直接影响。依赖微生物群的过程也被证明包括成人海马神经发生和小胶质细胞激活,即类似于免疫细胞的大脑和骨髓细胞的激活。”
自身免疫起源的实验模型表明肠道微生物组在这方面也起着重要作用。这一见解为寻找多发性硬化症(MS)的病因开辟了新的途径。MS是一种自身免疫性疾病,由遗传和环境因素共同导致。德国Martinsried Max Plank神经生物学研究所的Gurumoorthy Krishnamoorthy博士说:“显然,细菌可以触发多发性硬化症不是致病细菌,而是消化所需的有益细菌。”一项针对转基因小鼠的研究表明,肠道菌群正常且不受外界影响的动物会出现大脑炎症。相比之下,在无菌环境中的老鼠仍然健康。正如Krishnamoorthy博士解释的那样,肠道菌群正常的小鼠的免疫系统在两个阶段被激活:首先,t细胞变得活跃,并在肠道的淋巴管中繁殖。在一起
它们与髓鞘中的表面蛋白结合,然后刺激b细胞形成致病抗体。Krishnamoorthy博士说:“这两种疾病都会在大脑中引发炎症反应,从而分阶段破坏髓鞘,这与人类多发性硬化症的发病方式非常相似。”这一过程表明,导致ms的不是神经系统的紊乱,而是免疫系统的变化肠道微生物群在人类身上同样可以引起免疫系统对…反应过度髓鞘如果存在相应的遗传倾向。然而,目前还不清楚是哪种细菌参与了多发性硬化症的发展。
肠道微生物组
微生物群由多达1000种不同类型的细菌和大约100万亿个细胞组成。因此,它的细胞数量是人类基因组的10倍,基因数量是人类基因组的150倍。微生物群与它的人类宿主以共生关系共同进化。的发展肠道微生物组作为一个精细调节的生态系统取决于许多因素:一个人在出生时是否从他/她母亲的产道中吸收了哪些微生物;一个人是否受抗体影响;一个人吃什么食物;感染;压力和遗传倾向。健康状况不佳的老年人,其微生物群中的微生物多样性往往较低,或有促进炎症的表现。
进一步探索