UCSF团队发现了根除侵袭性乳腺癌的新方法
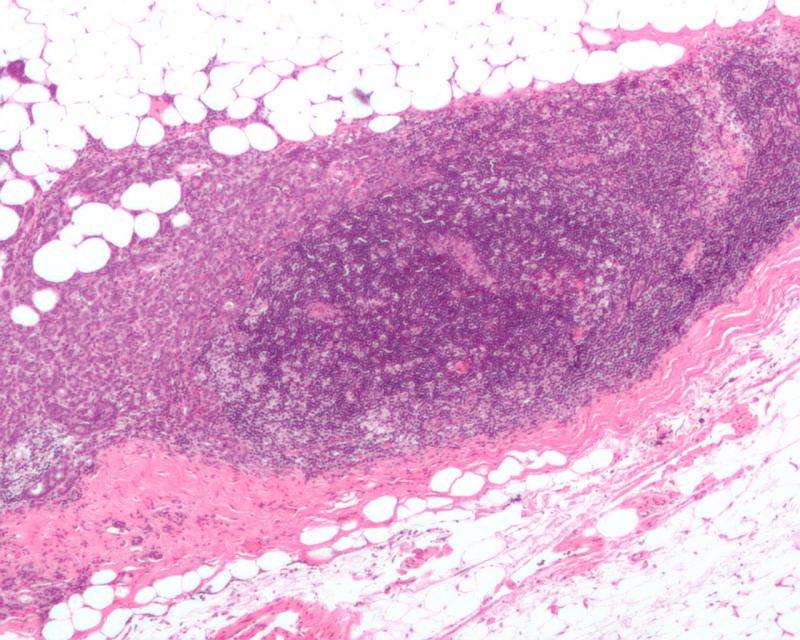
常规化疗通常不能根除侵袭性乳腺癌,因为这些疾病可能发生早期远处转移。三阴性乳腺癌(TNBC)是一种侵袭性特别强的亚型,目前尚无靶向治疗方法。最近发现,癌基因MYC在TNBC中升高,这为开发新的靶向治疗策略提供了有希望的机会,这些策略将允许选择性杀死MYC过表达的TNBC细胞。
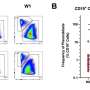
在国防部乳腺癌希望时代学者奖的支持下,Andrei Goga博士采取了多方面的方法来确定myc驱动的tnbc的新治疗靶点。在研究的第一部分,Goga博士的团队使用荧光激活细胞分选(FACS)试验从患者来源的乳腺癌异种移植模型(PDX)中分离出播散性肿瘤细胞(dtc)。dtc是不再存在于原发肿瘤但占据外周组织并可能发展为转移性肿瘤的癌细胞。基于人类细胞标志物CD298的表达,使用FACS对细胞进行分类,允许检测早期dtc以及来自晚期转移性肿瘤负担组织的dtc。然后用qPCR方法测定分离细胞的基因特征。
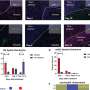
Goga研究小组发现,来自低肿瘤负荷组织的转移细胞具有增强的干细胞样基因特征,而来自高负荷组织的转移细胞显示出更接近原发肿瘤的特征。从低负荷区和高负荷区分离出来的细胞之间的一个重要区别是它们是否进入了细胞周期。来自低负荷组织的细胞显示出静止和休眠的标记,而来自高负荷组织的细胞显示出腔内分化的标记,这表明它们已经进入细胞周期,因此表达了MYC水平的升高。因此,来自高负荷组织的dtc被证明对周期蛋白依赖性激酶抑制剂dinaciclib敏感(Merck)。经过四周疗程后,24只药物治疗小鼠中只有1只发现了dtc,而25只载体治疗小鼠中有11只发现了dtc。此外,虽然药物治疗动物的原发肿瘤生长减慢,但许多动物在研究结束时仍有明显的原发肿瘤,这表明地那西利的抑制作用更大转移性肿瘤与原发肿瘤相比。
总的来说,这项研究的结果表明,在转移亚群中,MYC癌基因与原发肿瘤相比明显上调。使用CDK1/2/5/9细胞周期抑制剂治疗可耗尽播散性肿瘤起始性细胞用地那西利布治疗可以预防转移性乳腺癌通过消除MYC表达升高的dtc。这是一个重要的发现,因为dinaciclib治疗各种癌症的临床试验已经在进行中。
在研究的第二部分,使用靶向代谢组学方法,Goga博士的团队确定脂肪酸氧化(FAO)中间体在myc驱动的TNBC模型中显著上调。在MYC驱动的转基因TNBC模型和MYC过表达TNBC PDX模型中,他们发现对FAO的抑制降低了能量代谢并阻止了肿瘤生长,这表明FAO对体内肿瘤活性具有关键作用。这是第一个研究MYC在体内TNBC代谢中的作用的研究,结果证明了进一步研究抑制FAO作为TNBC患者的治疗策略。
更多信息:Roman Camarda等人,抑制脂肪酸氧化作为myc过表达三阴性乳腺癌的治疗方法,自然医学(2016)。DOI: 10.1038 / nm.4055
2015. Lawson DA, Bhakta NR, Kessenbrock K, Prummel KD, Yu Y, Takai K, Zhou A, Eyob H, Balakrishnan S, Wang C-Y, Yaswen P, Goga A, Werb Z.。单细胞分析揭示了人类转移性乳腺癌细胞中的干细胞程序。自然526(7571): 131 - 135。