用CRISPR/Cas9靶向感染疱疹病毒
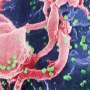
大多数成年人携带多种疱疹病毒。在最初的急性感染之后,这些病毒在宿主中形成终生感染,并导致唇疱疹、角膜炎、生殖器疱疹、带状疱疹、传染性单核细胞增多症和其他疾病。有些疱疹病毒能引起人类癌症。在感染的潜伏期,病毒在很长一段时间内保持休眠状态,但仍有能力引起偶尔的重新激活,这可能导致疾病。6月30日发表的一项研究PLOS病原体表明用CRISPR/Cas9基因组编辑技术攻击疱疹病毒DNA可以抑制病毒复制,并在某些情况下导致病毒的消除。
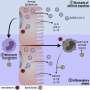
CRISPR/Cas9系统以特定的DNA序列为目标,在DNA的两条链上诱导干净的切割。在哺乳动物细胞中,这种切割被标记出来,并被一种叫做NHEJ(用于非同源端连接)的紧急修复系统迅速修复。NHEJ是有效的,但不是非常准确,经常导致插入或删除一些DNA碱基在修复位点。因为DNA是一次读取三个碱基的密码子,关键位置的这种微小变化往往会破坏相应基因及其蛋白质产物的功能。
荷兰乌得勒支大学医学中心的Robert Jan Lebbink和他的同事推断,CRISPR/Cas9可以靶向并突变感染人类细胞中潜伏的疱疹病毒DNA,因此有可能预防疱疹病毒相关疾病。为了验证这一点,研究人员设计了特定的引导rna (g)序列,它是病毒基因组重要部分的补充,并发挥“分子地址”的作用。这些gRNAs与CRISPR/Cas9系统的“分子剪刀”部分结合,应该会诱导疱疹病毒DNA的特定切割和随后的突变,从而削弱病毒。
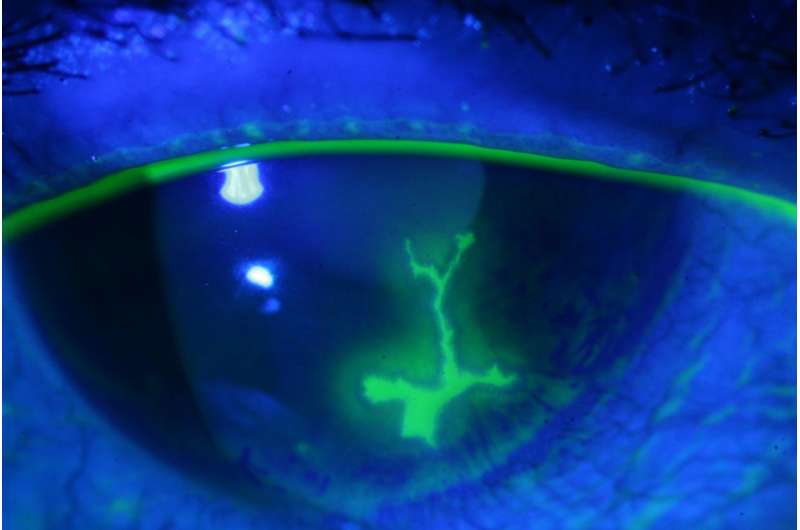
在他们的系统方法中,研究人员观察了疱疹病毒组的三个不同成员:单纯疱疹病毒病毒1型(HSV-1)引起唇疱疹和疱疹性角膜炎;人类巨细胞病毒(HCMV),最常见的导致出生缺陷的病毒(当病毒由母亲传播给胎儿);和eb病毒导致传染性单核细胞增多症和多种类型的癌症。
通过研究潜在感染EBV的淋巴瘤细胞,研究人员发现,引入靶向特定EBV DNA序列的gRNAs可以在靶向位点引入突变。这种突变可以消除病毒的基本功能,并使病毒DNA分子不稳定。与此一致的是,研究人员报告说,通过使用两种不同的靶向EBV基本基因的gRNAs,它们可以诱导宿主细胞中超过95%的EBV基因组的丢失。
潜伏感染期间,HCMV基因组以环状DNA分子的形式存在于宿主细胞的细胞核中。病毒重新激活后,HCMV复制进展缓慢。通过适当的gRNAs,研究人员发现CRISPR/Cas9编辑可以有效地削弱HCMV的复制。然而,他们也观察到逃逸变异的出现,绕过CRISPR/Cas9编辑,这表明在HCMV基因组的多个关键位点同时编辑是必要的,以避免耐药基因组的发展。
与HCMV相比,HSV-1的繁殖速度要快得多。当研究人员结合CRISPR/Cas9测试针对不同基本HSV-1基因的各种gRNAs时,他们发现其中许多gRNAs能够减少病毒复制。当他们结合这两个gRNAs,从而同时靶向两个基本基因时,他们能够完全抑制HSV-1的复制。另一方面,在潜伏阶段,即当病毒DNA不活跃繁殖时,它们无法诱导编辑。
研究人员总结说:“我们观察到从潜伏感染的肿瘤细胞中高效和特异性地清除EBV,并损伤人类细胞中的HSV-1和HCMV复制。”他们继续说,“尽管CRISPR/Cas9在指导静止HSV-1的基因组工程方面效率不高,但静止HSV-1重新激活后的病毒复制可以使用抗HSV-1 gRNAs有效地消除”。他们希望,他们的结果“可以设计出有效的治疗策略,在潜伏感染和产生感染期间针对人类疱疹病毒。”
进一步探索