疼痛医学模式有助于保护视力的遗传性视网膜变性
止疼药,强有力地激活受体视网膜至关重要的健康似乎有助于保护视力严重视网膜变性的模型中,科学家们报告。
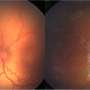
潜在的致盲性疾病如色素性视网膜炎和视网膜黄斑性病变导致视网膜感光细胞的损失,使我们能够将光转换成图像。
这项研究在《华尔街日报》美国国家科学院院刊》上表明,在严重的动物模型,遗传性视网膜变性,药物(+)镇痛新启用的生存圆状细胞,一种感光细胞,给我们详细,色觉,西尔维亚•史密斯博士说,细胞生物学和解剖学的主席奥古斯塔大学乔治亚医学院的。
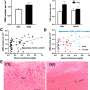
有一个“惊人的”保护锥函数影响小鼠治疗(+)-镇痛新,史密斯说,视网膜细胞生物学家、该研究的通讯作者。事实上,锥函数本质上是一样的在正常小鼠,而未经处理的突变小鼠的视力丧失的进展如预期。
白天42岁时视力应该是丢失了,几层感光细胞仍清晰可见的治疗小鼠和绝大多数的这些细胞是锥。老鼠缺乏西格玛受体1没有受益(+)-镇痛新治疗,更多证据受体的重要作用在视网膜的保护,史密斯说。治疗小鼠也减少氧化应激的证据。
虽然可能不是患者的首选药物这些问题,科学家们知道,(+)-镇痛新,止痛药证明似乎也有潜力改善失败的记忆,是一个强有力的σ1受体的激活。
仍在工作期间正是这样,overactivating西格玛受体药物可能增加活动的自然氧化蛋白质Nrf2,和其他潜在的机制,以更好地保护细胞,史密斯说。
也有证据表明,减少炎症,治疗通常伴随着氧化应激,以及内质网压力,一个重要的细胞器,帮助身体,褶皱和运输蛋白包括消除严重折叠的功能,因为他们不应该。
“氧化压力,尤其是在视网膜上,因为巨大的光,”史密斯说。视网膜感光细胞的光转换成信号,大脑转化成图像。但在大多数情况下,过多的光线也对我们的眼睛有害,特别是荧光仍然弥漫在许多业务设置,以及过度的阳光。
“视网膜需要光和氧气让我们看到,然而,可以破坏氧化环境,”史密斯说的新陈代谢要求感光细胞。“这是一个绳索。”In fact, a panel of her peer retinal cell biologists would likely say that oxidative stress is their biggest concern in terms of retinal degeneration, she said. Oxidation occurs when too many free radicals, a natural byproduct of oxygen use, are generated for the eye to eliminate through natural mechanisms and become lethal to cells.
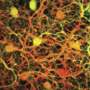
去年夏天,在《华尔街日报》自由基生物学和医学史密斯的实验室显示,σ1受体的作用在一个健康的视网膜。没有它,穆勒支持视网膜的细胞似乎无法控制自己的破坏性的氧化应激水平,因此,不能正确地支持数以百万计的特殊的神经元,使我们能够将光转换成图像。组织良好的层视网膜细胞开始瓦解,愿景是迷路了。
这一发现还发现了σ1受体作为一个潜在的治疗目标青光眼、糖尿病视网膜病变等失明的主要原因。她的实验室在2008年报道(+)-镇痛新似乎如何帮助多层视网膜保持其分层形式和功能和减少损失的神经节细胞,接收信息的神经细胞在视网膜上感光细胞。最外层含有色素上皮,这有助于滋养视网膜,和下一层了感光细胞。
感光细胞还包括棒,大多聚集在视网膜的周边,使夜间或晚上昏暗视觉。棒通常是在视网膜变性失去了第一次那么锥屈服的。
史密斯的许多问题和她的团队现在想回答是多久锥函数可以保存在老鼠用(+)-镇痛新治疗。
他们的模型是一个老鼠的基因突变,提示快速损失35天视杆细胞和视锥细胞的生活,是一个严重的遗传模型视网膜变性像色素性视网膜炎。他们将药物注入腹腔每隔一天在42天的生活。史密斯和她的团队现在还想确定最佳剂量。他们也想更好地了解药物在这么高的工作氧化应激环境。计划包括也把Nrf2从他们的突变小鼠进一步追求蛋白质是否参与这一场景。
更多信息:王静et al .激活的分子伴侣蛋白,σ1受体,保留了锥函数在遗传性视网膜变性的小鼠模型,美国国家科学院院刊》上(2016)。DOI: 10.1073 / pnas.1521749113