新的研究增加了潜在的治疗目标证据β淀粉样蛋白在阿尔茨海默氏症
新的研究发现认知神经学中心的纽约大学Langone医学中心可以提供额外的线索为未来治疗目标推迟老年痴呆症和相关的痴呆症。这是根据集团最新的发现将会在阿尔茨海默病协会国际会议(AAIC), 7月24日到7月28日在多伦多。
阿尔茨海默病,最常见的痴呆症,是一种无法治愈的,退行性疾病导致内存问题,思维和行为。阿尔茨海默病和其它痴呆影响全球4700万人和530万人,数字,预计三到2050年,根据阿尔茨海默氏症协会。在这个时候,没有治愈但研究等,提出了AAIC会议旨在寻找延迟出现症状,改善患者的生活质量,并可能最终为更多治疗铺平道路。
预防的新目标
新的纽约大学Langone在老鼠身上的研究人员可能为临床试验来测试药物铺平道路被称为碳酸酐酶抑制剂(中美国际学校)作为潜在的治疗阿尔茨海默氏症,目标背后的机制被认为是神经和血管死亡通常与疾病相关。
现在人们普遍认为,线粒体dysfunction-a细胞器的破坏,调节细胞能量代谢和死亡——触发神经和血管的发展许多老年痴呆症患者死亡。线粒体功能障碍是引起的累积淀粉样β蛋白,反过来导致斑块积聚在大脑中。
在他们的研究中,纽约大学Langone研究者发现蔡medications-previously经美国食品和药物管理局(FDA)等其他条件glaucoma-target这背后的机制障碍。
“疗法旨在防止线粒体失败可能代表有前途的新策略我们寻找治疗这种毁灭性的疾病,“主要研究作者说西尔维亚Fossati,博士,纽约大学Langone神经病学和精神病学助理教授。
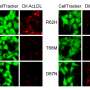
在这项研究中,Fossati和他的同事们看着两个fda批准的中美国际学校:methazolamide和乙酰唑胺。第一次,这些药物在细胞培养和小鼠模型进行测试,显示大脑中β-淀粉样蛋白的形成,称为淀粉样变。在淀粉样变性的小鼠,研究人员首次显示这些药物对记忆的积极影响,淀粉样蛋白沉积还存在,激活的酶称为驱动细胞死亡机制在大脑中。
研究人员认为,这些化合物的保护作用可能是由于线粒体功能障碍的预防,以及脑血流量的影响称为活化剂,产生更有效的消除β淀粉样蛋白的蛋白质从大脑。进一步的研究旨在测试类似的化合物在动物模型中,由于这些药物已经fda批准,Fossati补充说,未来的研究可能涉及的规划快速临床试验早期阿尔茨海默氏症或轻度认知损害(MCI)患者。
免疫疗法用于减少蛋白质β淀粉样蛋白的含量
通过免疫疗法减少β-淀粉样蛋白在以前的小鼠研究显示有好处。然而,一项新的研究,由马丁·萨多夫斯基博士,神经学副教授,精神病学和生物化学和分子药理学,纽约大学Langone表明,需要更多的研究来减少潜在的风险,这可能有效的治疗方法。
基因变异的载脂蛋白E (APOE)映射到一个特定的基因染色体19日最重要的因素是预测对阿尔茨海默病的易感性增加引起的β淀粉样蛋白斑块。有三种变体的载脂蛋白e: APOEε2 APOEε3和APOEε4。先前的研究已经表明,变异APOEε4显著增加阿尔茨海默氏症的风险,而APOEε2疾病降低风险;APOEε3是鲜为人知的影响。估计有20%的人携带可能加大APOEε4基因变异。
免疫治疗研究针对β淀粉样蛋白斑块积聚,但以前的研究已经表明载脂蛋白eε4受试者倾向于开发特定的不利影响被称为淀粉样蛋白相关的成像异常(咏叹调),包括micro-hemorrhages、大脑或出血,鉴于这种治疗。
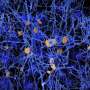
和他的同事在这项新的研究中,萨多夫斯基对β淀粉样蛋白免疫治疗的效果在阿尔茨海默病转基因老鼠,设计有三种人类APOE基因变异。他们找到了一个更大的免疫治疗对减少小鼠的β-淀粉样蛋白沉积的负载表达APOEε4变种比其他老鼠表达APOE变体。β-淀粉样蛋白沉积的间隙增加激活大脑中的小胶质细胞有关,吸收和消化淀粉样β蛋白。小胶质细胞的激活在小鼠表达更大的APOEε4变种比其他老鼠表达APOE基因变异,这可能会导致有害的刺激小胶质细胞对大脑的影响。
研究人员还发现,在转基因小鼠老年痴呆症,APOE变体有着不同的影响β淀粉样蛋白沉积在大脑的血管壁上,与APOEε4促进大型船只的β淀粉样蛋白的沉积,APOε2导致更多的β淀粉样蛋白沉积在大脑的micro-vessels。
β淀粉样蛋白的免疫疗法清除大脑血管,但它与增加脑部出血的发生率。最大的脑出血的发病率是APOEε2中发现老鼠而最低APOEε3中发现了老鼠。
这些新发现提供了前所未知的信息可能会帮助免疫治疗阿尔茨海默氏病的发展。
“我们的研究确定了之前被低估了risk-promoting APOEε2和APOEε3的保护作用相关的脑部出血的发病率淀粉样β蛋白。免疫,”萨多夫斯基“这是一个重要的小鼠模型,观察可能影响免疫疗法治疗,如疫苗,对阿尔茨海默氏症在人类开发和测试一天。”