团队发现线粒体应激诱发癌症相关的代谢变化
美联储必须癌瘤。他们不受监管的发展需要一个稳定的血流和营养。因此,一种方法,研究人员试图消灭癌症是靶细胞进行代谢变化,使肿瘤的快速生长。
然而,来自宾夕法尼亚大学的研究人员新发现表明这些努力可能错过了一个重要途径,使新陈代谢的变化有利于肿瘤。独自工作发现,线粒体压力会引发代谢变化通过一个涉及p53通路,一种蛋白质广泛扮演着多种重要作用于癌症。
“在所有5个癌症细胞系我们看,我们发现p53诱导时线粒体功能受到影响,”资深作者Narayan说Avadhani,哈丽雅特·埃里森伍德沃德的宾夕法尼亚大学兽医学院的生物化学教授的生物医学科学。“这导致我们的发现有可能促进肿瘤生长的独立HIF-1α通路,曾到目前为止治疗干预措施的主要目标。”
这项研究指出了一个新的因素,可以通知我们了解癌症的进展。有可能的标记代谢压力甚至可以作为生物标志物癌症的攻击性或传播可能性。
Avadhani与宾夕法尼亚大学兽医Chowdhury Anindya罗伊,第一作者和研究助理,哔叽y Fuchs,细胞生物学教授和博士生苹果长Anil Rustgi胃肠病学t·格里尔·米勒教授,宾夕法尼亚大学佩雷尔曼医学院的。Avadhani和福克斯也宾夕法尼亚大学兽医的Mari劳比较肿瘤中心。
这项工作发表在杂志上致癌基因。
在早先的研究中,Avadhani和他的同事们表明,破坏线粒体可能导致肿瘤的生长。线粒体通常被称为细胞的“强国”,因为他们产生ATP分子能量货币细胞利用来执行不同的功能。在相关工作中,研究人员还发现,对线粒体压力也引发了p53的增加,但直到现在,没有进行后续发现。
因为p53突变在近50%的人类癌症,人们普遍认为肿瘤抑制功能。研究人员决定采取详细看看线粒体压力和p53之间的联系。
他们实验耗尽线粒体DNA诱导线粒体压力在六个细胞系,包括一些癌症细胞系,发现p53水平增加应对mtDNA损耗在每种类型的细胞。因为HIF-1α活动扮演着互补和相互矛盾的角色在癌症p53,他们下了看看,蛋白质反应。他们发现p53抑制HIF-1α活动。
专门看人类结肠癌细胞系p53的实验性地删除,他们又发现了一个与HIF-1α关系:其活动高出6在结肠癌细胞系比野生型p53耗尽结肠癌细胞系,进一步表明p53抑制HIF-1α。
确保这不是严格与损耗的线粒体DNA,研究人员诱导线粒体应激使用其他方式,包括化学品代理通过破坏细胞膜,并发现p53诱导。
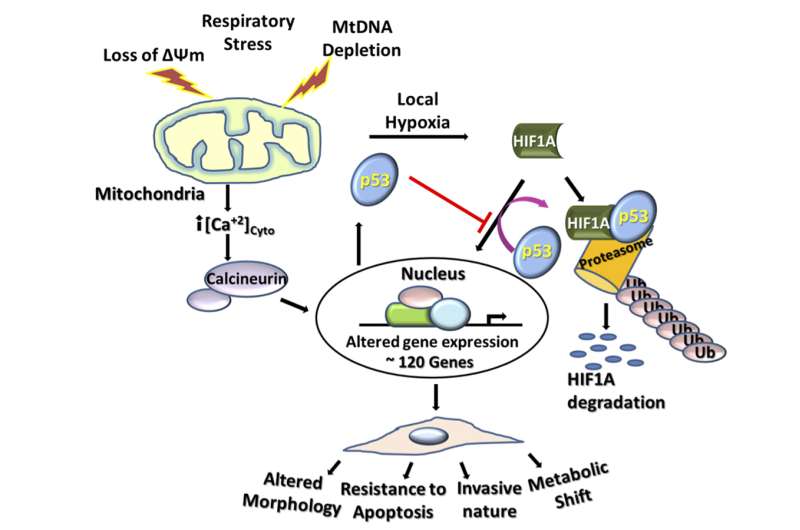
进一步调查表明p53 HIF-1α水平降低在细胞核和细胞质的细胞和基因响应HIF-1α能减弱线粒体DNA耗尽的时候。值得注意的是,他们发现多个基因的表达参与糖酵解,一个细胞分解糖的代谢过程能量,大幅跃升的细胞mtDNA耗尽。其中一些是相同的基因通常HIF-1α调节,指着线粒体压力作为一个相似但完全独立的途径代谢转变可以发生在癌症细胞。
最后,团队证明,与贫化mtDNA细胞,p53物理干扰HIF-1α通过阻止它绑定到基因启动子,它通常会和通过促进HIF-1α泛素化,这一过程标记细胞蛋白质的降解。
研究结果指出新的方向和可能的新的目标对预防代谢转变可以促进肿瘤生长一个支持性的环境。
“我们表明,线粒体应激是一个不容小觑的力量,“Avadhani说。“如果人们只关注HIF-1α防止新陈代谢的变化,这可能是不够的。线粒体应激能引起所有这些变化。”
Avadhani和他的同事们在追求这些领导,致力于设计治疗干预的目标分子标记线粒体压力,试图阻止代谢转变,可以帮助养活实体肿瘤。
进一步探索





用户评论