致盲疾病在狗和人类股票诱发基因,病理变化
Ciliopathies疾病影响纤毛,感官细胞器,大多数哺乳动物细胞具备并发挥重要作用在很多生物功能。一个这样的疾病是高级Løken综合症的一种罕见的疾病,可能涉及严重的肾病和致盲疾病雷伯氏先天性黑内障,或LCA。
十年前,来自宾夕法尼亚大学的研究人员和他的同事发现了一只狗和一个类似的眩目的条件下,2013年,他们报道的致病基因。
现在宾夕法尼亚大学科学家们报告说,他们已经直接比较了人类和狗之间疾病过程,发现惊人的相似之处。
鉴于动物模型的至关重要的作用,在推动疾病的治疗方法,研究人员发展持乐观态度第一狗疗法治疗条件,并最终在人。
“当我们开始描述疾病时,我们发现惊人的相似之处的一个子集LCA患者人类和狗的突变,“古斯塔沃·d·Aguirre说,文章的第二作者,医学遗传学和眼科教授宾夕法尼亚大学兽医学院的。“我们非常热情的潜在缩小这种疾病治疗窗口并开始测试转化疗法。”
该研究发表在《华尔街日报》人类分子遗传学从佩恩和包括一个跨学科的团队。除了Aguirre,宾夕法尼亚大学兽医贡献者包括文章的第二作者威廉·a . Beltran co-first作者路易丝·m·唐斯和艾琳·m·斯科特·西蒙腺上皮,瓦莱丽·杜福尔,克里斯汀·l·加德纳、Sem Genini和路易斯·菲利普马里奥。作为长期合作的一部分,佩雷尔曼医学院Scheie眼科研究所,Aguirre, Beltran)的团队与阿图尔诉Cideciyan塞缪尔·g·雅各布森和亚历山大•Sumaroka Mychajlo Kosyk和马格达雷娜Swider。杰弗里·k·Aguirre的佩雷尔曼医学院的研究团队,贡献他的专长在神经学、神经因素可以出现在人类形体的综合症。
当潘团队帮助发现ciliopathy狗,他们注意到一些不寻常的东西。
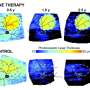
“犬类疾病最引人注目的是,尽管狗缺乏功能性视觉在白天,“Aguirre说,“视锥细胞,在日光下的感光细胞,仍然存在。”
“它们,但它们在结构上很妥协,“添加Beltran),在宾夕法尼亚大学兽医眼科副教授。“现在的关键问题是回答是治疗不仅会阻止退化过程但修复这些异常锥和视力恢复的一天。我们有令人兴奋的初步基因治疗结果似乎证实,这确实是可能的。”
在2011年的一项研究中,兽医人员Cideciyan Scheie研究所的同事,雅各布森,眼科宾夕法尼亚大学医学教授,在他们的一些观察到的类似人类的LCA的患者。他们的中央视网膜视锥细胞包含保存但缺乏功能。杖感光细胞,负责昏暗的灯光视觉,在生命早期恶化。
这些人与狗ciliopathy,同样的基因参与了:NPHP5。发现该基因突变是如何影响视锥细胞功能和杆恶化,研究人员转向犬模型。
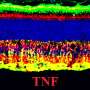
艾琳·斯科特,当时一个兽医学生双方对默克/研究学者Beltran)的实验室,和露易丝Aguirre的实验室的一位博士后研究员,跟踪狗的疾病,在人类寻找相似的模式。锥细胞仍然存在,尽管非功能性和结构性改变,直到很晚,大约42周的年龄,当他们逐渐退化。他们观察到在生命的早期,大约六个星期,大多数受影响狗的视锥细胞未能形成外段,由纤毛内部连接段,光捕获光感受器的结构。内段也出现无序,类似的报道在人类患者。
研究人员调查了112个基因的表达在视网膜上已知的发挥直接作用的视野,参与细胞死亡或生存,看看NPHP5变异如何影响他们。他们发现在NPHP5变异狗在33这些基因表达的变化也改变了另外两个狗的一些形式的视网膜变性。
最后,研究者评估是否与突变在人类NPHP5,肾脏功能或结构受到影响,但发现狗似乎并未受到这些ciliopathic综合症的其他特性的影响。
通过基因治疗研究提供一个正常的副本NPHP5犬模型的基因疾病已经开始与前途的早期结果。
更多信息:路易丝·m·唐斯et al,重叠的异常感光发展和进步变性雷伯氏先天性黑内障bymutation引起的,人类分子遗传学(2016)。DOI: 10.1093 /物流/ ddw254