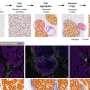
研究确定了小说在BRAF-mutant黑色素瘤治疗耐药机制
马萨诸塞州总医院(MGH)的一个研究小组发现了一个额外的抗BRAF-mutant靶向治疗黑色素瘤的机制。他们的论文,接受提前在线出版自然医学报告说,灭活两个基因的突变负责调节细胞分裂的关键方面可以激活的信号通路导致肿瘤的生长被BRAF抑制剂药物。
“我们发现的肿瘤抑制STAG2或STAG3 BRAF抑制剂是一种新型的遗传机制电阻还揭示了一个意想不到的联系这些蛋白质和MAPK细胞生长途径,激活驱动这些肿瘤,”本郑博士说,皮肤的生物学研究中心在MGH,论文的通讯作者。“理解和克服阻力BRAF抑制黑色素瘤领域面临的仍然是一个主要挑战。识别能力的生物标志物预测响应BRAF抑制剂药物-如vemurafenib和dabrafenib将促进早期发现病人可能从治疗中获益,使监测耐药性的发展,可以考虑其他的治疗方案之前复发。”
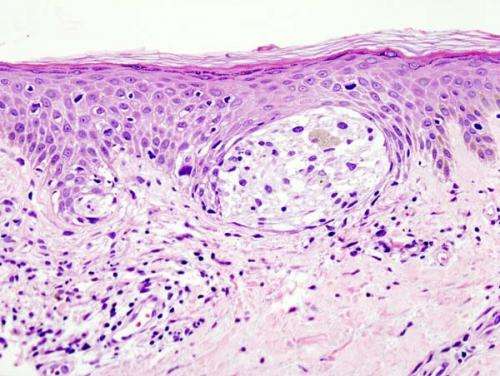
在恶性黑色素瘤病例的一半——最致命的皮肤癌肿瘤生长是由BRAF基因的突变,和治疗的肿瘤药物抑制BRAF活动可以在大多数情况下逆转肿瘤的生长。但治疗抵抗几乎总是发展,导致重启肿瘤的生长。这背后机制抵抗几件物品已经被确认,包括在其他基因突变MAPK通路,BRAF的一个组件,它基本上避免了抑制BRAF活动。但多达25%的情况下的阻力BRAF抑制剂不涉及识别机制。
在寻找额外的耐药机制,研究人员首次演出whole-exome测序的病人的肿瘤样本前处理和后抵抗vemurafinib BRAF抑制剂的发展。比较新颖的突变post-resistance样本的已知的癌症相关的基因突变确定一个显著变异肿瘤抑制基因STAG2。基因及相关基因叫做STAG1 STAG3代码单元的cohesin复杂,组装的蛋白质调节细胞分裂的必经阶段,染色体的分离,也可能在基因表达的调控中发挥作用。几个cohesin复杂的基因,包括STAG2已知突变在其他形式的癌症。郑指出,蛋白质是如何发挥其肿瘤抑制功能在任何类型的癌症尚未确定。
检查小组的所有三个鹿蛋白质水平难治性黑色素瘤细胞系确定减少表达STAG2 STAG3几行,包括一些被抗抑制BRAF和MEK的MAPK通路中的另一种蛋白质。他们发现了什么可能是负责STAG2突变,虽然他们找不到任何STAG3突变面板,检查数据从BRAF抑制剂治疗之前发表的一项研究发现STAG3突变预处理样品很快耐药性的肿瘤治疗。
实验在培养黑素瘤细胞系和肿瘤植入小鼠显示击倒的蛋白质的表达减少敏感性通过重新激活BRAF抑制MAPK通路的后期。相比之下,越来越多的表达STAG2或STAG3 BRAF-mutated黑色素瘤细胞增加vemurafinib治疗的有效性。
“观察突变STAG2或STAG3可能导致重新激活MAPK通路的小说和意想不到的发现我们的研究,”郑说,他是哈佛大学医学院皮肤学助理教授。“我们现在工作识别漏洞STAG2/3突变黑色素瘤和发现新的方法来瞄准这些肿瘤,我们希望将提供新的见解预防BRAF抑制剂阻力和治疗肿瘤已成为耐药。”
更多信息:失去cohesin复杂组件STAG2或STAG3抵抗BRAF抑制黑色素瘤,自然医学,DOI: 10.1038 / nm.4155