基因组工程为镰状细胞治疗铺平了道路
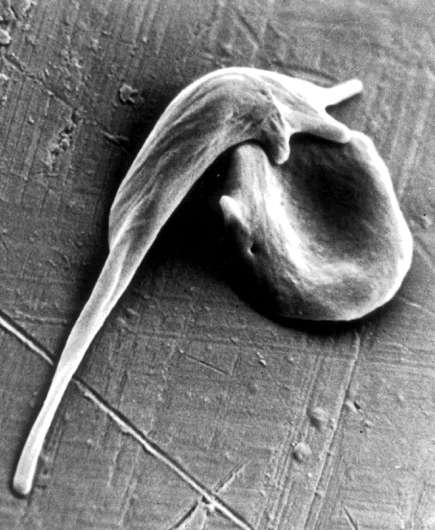
一个医生和实验室科学家团队对镰状细胞疾病的治疗方法进行了关键步骤,使用CRISPR-CAS9基因编辑来修复受影响患者血液中干细胞中疾病的突变基因。
这是第一次,他们纠正了一部分干细胞的突变,这些干细胞的比例高到足以在镰状细胞患者中产生实质性的益处。
加州大学的研究人员,UC旧金山班里夫儿童医院奥克兰研究所(Chori)和犹他大学医学院希望重新注入患有编辑的干细胞,并减轻疾病的症状,主要是折磨非洲血统,导致贫血,痛苦的血液堵塞和早期死亡。
“我们非常兴奋,对这项技术的承诺,”UC Berkeley的创新基因组学倡议研究和科学主任的高级作者Jacob Corn说。“在诊所使用这种方法之前,仍有很多工作要做,但我们希望它将为患者提供新的治疗方法镰状细胞病”。
在小鼠的测试中,转移后的转基因干细胞在移植后至少四个月地粘在一起,这是一种重要的基准,以确保任何潜在的治疗都会持久。
“这是一个重要的进步,因为我们首次展示了干细胞的矫正水平,应该足以在患有这种疾病的人身上产生临床效益。镰状细胞性贫血合著者Mark Walters说,他是一名儿科血液学家和肿瘤学家,也是UCSF奥克兰贝尼奥夫血液和骨髓移植项目的主任。
结果将在10月12日发行在线期刊上报告科学转化医学。
镰状细胞病是一种隐性遗传疾病,由乙型球蛋白(一种构成携氧分子血红蛋白一部分的蛋白质)的两个基因拷贝的单一突变引起。这种纯合子缺陷导致血红蛋白分子粘在一起变形红细胞成为一个特征的“镰刀”形状。这些畸形细胞粘在血管中,造成障碍,贫血,疼痛,器官衰竭和寿命大大缩短。镰状细胞疾病在非洲裔美国人和撒哈拉以南非洲人口尤其普遍,影响全球数十万人。
这个多机构团队的目标是开发基于基因组工程的方法,以纠正每个患者自身干细胞中的致病突变,以确保新的红细胞是健康的。
该团队使用CRISPR-Cas9来纠正造血系统中的致病突变干细胞——成熟为红细胞的前体细胞——从镰状细胞患者的全血中分离出来。修正后的细胞产生健康的血红蛋白,而突变后的细胞则根本不产生血红蛋白。
研究人员强调,未来的临床前工作将需要额外的优化,大规模的鼠标研究和严格的安全分析。玉米和他的实验室已加入Walters,一个专家开发患有骨髓移植和镰状细胞病的基因治疗等疗法治疗,以启动早期临床试验,以在未来五年内测试这种新的治疗。
值得注意的是,研究小组可能能够应用这项研究中描述的方法来开发其他血液疾病的治疗方法,如β-地中海贫血、严重联合免疫缺陷(SCID)、慢性肉芽肿疾病、罕见疾病如Wiskott-Aldrich综合征和Fanconi贫血,甚至艾滋病毒感染。
“镰状细胞病只是由基因突变引起的许多血液疾病中的一种,”考恩说。“其他研究人员和临床医生很有可能利用这种基因编辑来探索治愈大量疾病的方法。”
“为某些疾病发展疗法有明确的道路,”犹他大学联合高级教会Carroll表示,在十年前共同开发了第一次基因组编辑技术之一。“看看是非常令人欣慰的基因编辑技术被带给实际应用。“
这项工作是创新基因组学倡议的果实,UC Berkeley和UCSF之间的共同努力,旨在使用CRISPR-CAS9纠正利用CRISPR-CAS9的人类疾病的DNA突变,这是由UC Berkeley的科学家开发的开创性技术,该技术已经制定了基因组编辑比以往任何时候都更容易和更高效。
该项目还利用了UCSFBenioff儿童医院奥克兰的医生和科学家的专业知识,这是镰状细胞病的主要研究和治疗中心,以及Carroll在基因组工程领域的专业知识。
进一步探索













用户评论