新的靶向化疗小鼠的技术证明有效
旧金山加州大学的研究人员已经开发出一种新的化疗药物各种定位系统基于自由铁含量异常高的许多癌症cells-distinct蛋白结合的铁是常见的在整个身体的细胞。在实验小鼠和癌症细胞系,研究人员成功地选择性地杀死癌细胞,同时避免化疗的典型健康细胞毒性作用,从而刺激了容许剂量高达50倍。
新方法包括封闭保护化学框架内有效的化疗药物,只有遇到的高铁环境释放药物的肿瘤有可能添加一个有价值的新工具,肿瘤学家的越来越精确的制药阿森纳,使他们的目标和更高剂量的癌症化疗药物同时大大降低了折磨人的副作用。
“鉴于化疗在癌症治疗的主要作用,我们必须继续寻找方法来提高其疗效,减轻副作用,通常可以衰弱的病人,”艾伦·Ashworth说博士,总裁FRS UCSF海伦Diller家庭综合癌症中心。“这些发现是令人兴奋和有前途的,因为他们提供线索利用肿瘤耐药性的漏洞而阻挠和复发。”
这项新的研究,发表在其最终版本在线12月12日,2016年医药化学杂志,是在实验室里进行的亚当•Renslo博士,加州大学旧金山分校的副教授医药化学和海伦·迪勒家庭综合癌症中心的成员,由然后学生本杰明·斯潘格勒博士学位。
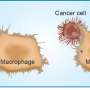
“传统化疗药物很有效地杀死细胞,但通常他们不是非常挑剔,这就是为什么病人经历如此可怕的副作用,”Renslo说。”相比之下,新的oncogene-targeted药物更有选择性,但是他们通常只对特别有效形式的cancer-plus,肿瘤往往能够发展阻力和复发。这种新方法结合的一些好处:它有不可避免的破坏力的化疗,但目标选择性癌症细胞。"
新tumor-activated前体药物是仿照iron-triggered抗疟药物
这项新的研究源于Renslo与合成抗疟药物的早期作品的灵感来自于自然产品和抗疟药物青蒿素,选择性攻击疟原虫的传感自由二价铁的高浓度heme-a铁的活性形式,是罕见的在正常细胞和组织的消化间hemoglobin-eating寄生虫。接触这个活性自由铁触发器在青蒿素的化学反应,导致有毒的副产品,杀死寄生虫。
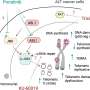
Renslo和他的同事们致力于创建一个新类的、有针对性的prodrugs-a术语药物如果被吞食是有惰性的,但身体内触发成为活跃的过程设计分子支架,它们被称为硫氧还蛋白,只有分裂和释放的活性形式自由二价铁的存在。
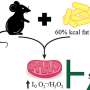
科学家早已知道,恶性肿瘤细胞同样含有高浓度的自由铁的结果自然跃跃欲试的新陈代谢所需的肿瘤细胞快速分裂和传播。测试是否iron-activated前体药物可能目标癌症,他们适应硫氧还蛋白分子携带两种不同的极有效的化疗药物和测试他们对各种癌症细胞系和两种不同的癌症的小鼠模型。
“我们选择两个非常强大的和有毒化学物质的目的,“Renslo说。“这些化合物是有毒,无选择性的使用自己的病人,但是我们想表明,即使这些药物可能是安全有效的,如果他们可能是针对肿瘤。”
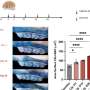
作者表明,硫氧还蛋白支架成功阻止了这些药物的毒性在健康细胞培养,但发布其有毒货物时引入多样化癌症细胞系。非癌细胞最初受药物的影响成为敏感当研究人员介绍了基因突变导致他们走向恶性状态。
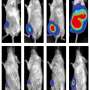
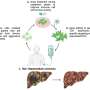
最后,研究人员测试了其中一个tumor-activated高活性化合物在鼠标异种移植模型中,人类癌症的嫁接到实验室的老鼠。他们建立了非常小的有毒化疗剂以外的肿瘤,被释放,因此,老鼠可以容忍一个剂量的药物前体50倍高于化疗剂。高剂量的组合和前体药物的改进针对癌细胞导致强劲和持久的减少这些老鼠的肿瘤。
“有很多这种方法使得其诊所之前,“Renslo补充道。“我们现在想了解哪些类型的癌症,这可能最大的影响——也就是说,那些没有有效治疗药物,和那些在自由特别高铁,因此可能会有效地激活高活性化合物。”
新方法的一个方面,尤其令人兴奋researchers-though是迄今为止untested-is癌症不太可能发展阻力iron-targeted化疗。
“据我们所知,恶性癌症必须获得并维持高亚铁为了自由复制和传播,“Renslo说。“他们不能切换到另一个金属用于这些目的,因此任何突变的癌细胞,减少了自由铁足以避免触发前体药物也可能会使细胞不那么咄咄逼人。我们认为没有地方可以躲。”
更多信息:本杰明斯潘格勒et al。小说Tumor-Activated前体药物战略目标亚铁是有效的在多个临床癌症模型,医药化学杂志(2016)。DOI: 10.1021 / acs.jmedchem.6b01470