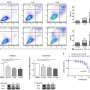
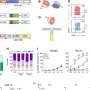
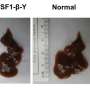
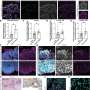
为什么对恶性血细胞癌AML的标准治疗经常失败
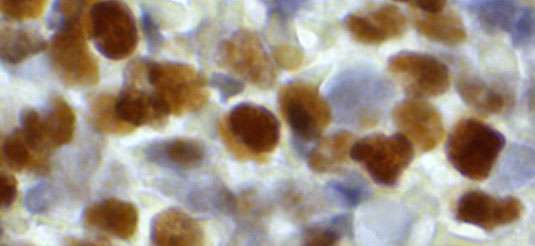
一个国际研究小组揭示了为什么侵略性血细胞癌AML的标准治疗经常失败。这项研究发现了一种新的生物标志物,可以预测化疗的疗效,并确定一种新的药物靶点。
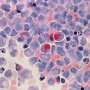
急性髓系白血病(AML)是一种癌症,其特征是某些类型的细胞不受控制地增殖白细胞.该疾病由广泛的突变引起,不同患者群体之间的预后也相应不同。所有组的标准治疗包括阿糖胞苷(阿糖胞苷)治疗,这是一种所谓的核苷类似物。大多数患者最初对化疗有反应,但许多患者长期失败,甚至对药物产生耐药性。耐药性导致复发和疾病进展的恢复。现在,由LMU Max von Pettenkofer研究所病毒学主席Oliver T. Keppler和法兰克福大学医学病毒学研究所教授Jindrich Cinatl Jr. (Keppler在2015年转到LMU之前是该研究所的主任)领导的一项研究确定了阿糖苷耐药背后的机制。
阿糖胞苷被细胞迅速吸收,并通过添加所谓的三磷酸基(一个小的化学基团)来进行化学修饰。事实上,这种药物的改良形式就是治疗活性物质。一旦被纳入复制癌细胞的基因组,它就会在细胞分裂过程中抑制进一步的DNA合成。恶性细胞通常分裂得非常快,因此比体内大多数其他类型的细胞更容易受到其有害影响。这项新研究发表在主要期刊上自然医学,鉴定出SAMHD1酶作为阿糖胞苷作用的抑制剂,并证明它通过从活性药物中去除三磷酸而起作用。
上下文相关的角色
Oliver Keppler的研究实际上集中在感染人类免疫缺陷病毒1 (HIV-1)后导致艾滋病发展的机制上。所以他在抗逆转录病毒治疗的背景下已经熟悉了SAMHD1,这也涉及到核苷类似物。为了在人类细胞中成功复制,HIV-1必须首先通过一种称为逆转录的过程将其RNA基因组转化为DNA。像DNA复制一样,RNA的逆转录可以通过将核苷类似物合并到正在生长的HIV-1 DNA链中而中断。没有完整的病毒DNA副本,就不能产生新的病毒颗粒。在这种情况下,SAMHD1被认为通过降解病毒所需的正常DNA构件来促进对病毒复制的抑制。
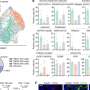
LMU的研究人员和法兰克福的合作者首先假设,类似的机制可能在阿糖胞苷处理的AML细胞中起作用,并且SAMHD1会增强类似物的效果。但事实证明,情况恰恰相反。“令我们惊讶的是,我们发现阿糖胞苷的活化形式本身就是SAMHD1的底物,”Keppler说:这种酶使药物失活,从而抑制了其抑制DNA合成的能力。“此外,有迹象表明,这种酶也可能以同样的方式与用于肿瘤治疗的其他核苷类似物的三磷酸相互作用。Keppler和他的团队与一大群临床医生、病理学家、药理学家、生物化学家和生物统计学家合作,继续表明——基于AML小鼠模型和AML患者的回顾性调查——SAMHD1确实是阿糖胞苷治疗这类白血病失败的关键因素。正如作者在新论文中所述,SAMHD1提供了一种细胞生物标志物,用于评估基于核苷类似物的治疗的潜在疗效,并在单个患者AML的进展中发挥重要作用。进一步的研究可能会指出抑制SAMHD1本身活性的方法,这将有望提高一类重要抗肿瘤药物的有效性。
更多信息:Constanze Schneider等人。SAMHD1是阿糖胞苷反应的生物标志物,也是急性髓系白血病的治疗靶点,自然医学(2016)。DOI: 10.1038 / nm.4255