在小鼠身上进行的实验可能有助于促进fda批准的脊髓性肌肉萎缩的新疗法
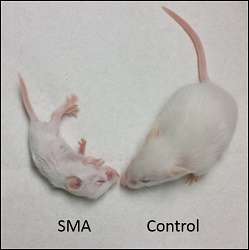
约翰霍普金斯大学的研究人员以及学术界和制药行业的研究人员表示,他们已经确定了一种治疗脊髓性肌萎缩症的新生物靶点。他们报告说,他们有证据表明,一种针对这一目标的实验药物与一种名为Nusinersen的药物联合起了“助推器”的作用,Nusinersen最近被fda批准用于改善小鼠的疾病症状。
在一份关于这项工作的报告中,发表在神经元12月23日,研究人员表示,联合疗法改善了患者的生存时间、体重和运动能力老鼠与脊髓性肌萎缩这是一种相对罕见的遗传性疾病,其特征是失去运动神经元或控制运动的神经细胞。
Nusinersen于2016年12月获得美国食品和药物管理局(fda)批准,成为首个获批治疗脊髓损伤的药物肌肉萎缩其他几种实验性药物仍处于临床试验阶段。约翰霍普金斯大学的研究人员和他们的同事说,如果进一步的研究证实,“增强”的nusinersen疗法有可能显著改善脊髓性肌萎缩症患者的生活,其中一些人的生命只有几周或几个月,还有一些人无法坐、站或行走。
研究人员警告说,他们在新研究中使用的增强疗法短期内不会上市,甚至不会用于人体试验;它必须先等待数年的动物试验来验证安全性和有效性。但他们补充说,他们的研究结果至少提供了一种扩展nusinersen效用的途径。
“fda批准的新药nusinersen可能有‘天花板效应’,因为它可能不能完全治疗这种疾病,”约翰霍普金斯大学医学院神经病学副教授夏洛特·萨姆纳(Charlotte Sumner)说。“我们的方法是与那些开发了nusinersen的人合作,以确定一种方法来提高他们的药物对病情最严重的患者的效果。”
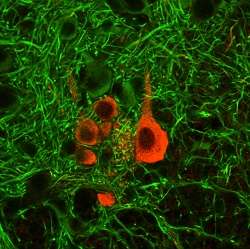
脊髓性肌萎缩是婴儿的主要遗传杀手之一,其原因是神经元中缺乏足够的生存运动神经元(SMN)蛋白。这种疾病是由SMN1基因的基因突变引起的,SMN1基因是SMN的蓝图,SMN是一种对发育很重要的运动神经元蛋白。每40个人中就有一人携带脊髓性肌肉萎缩症的缺陷基因,世界上所有种族的婴儿中,每6000个婴儿中就有一个出生时患有这种疾病。

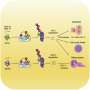
当研究可能影响神经元中SMN蛋白水平的机制时,研究人员扫描了一个名为UCSC基因组浏览器的基因组数据库,并确定了两个与SMN基因的相反DNA链相匹配的基因序列。通过分析DNA序列的程序,他们确定它们组成了一个长RNA。然而,这种类型的RNA是不同的,因为它不像传统基因那样组成或编码蛋白质的指令,而是“非编码”的。
研究人员在人类胚胎肾细胞、脑细胞样本和来自健康人以及I型和II型脊髓性肌肉萎缩患者干细胞的神经元中检测到了这种SMN长非编码RNA,或简称为lnc-RNA(读作“link RNA”)。在健康的人和小鼠中,研究人员观察到SMN蛋白在出生前处于高水平,出生后下降。研究人员注意到SMN lnrna的相反模式;在人类脊髓样本中,它在出生前处于低水平,但在出生前升高。他们在胚胎小鼠中也证实了这些相同的相反模式的SMA蛋白和SMN lnc-RNA。
然后,研究人员通过沉默或去除SMN lnna,寻找一种方法来增加SMA基因产物水平,信使rna (mRNAs),从而增加蛋白质水平。为了做到这一点,他们创造了8个不同的DNA片段,与相反的链相匹配,或者是SMN lnrna的反义版本,它会与lnrna结合并导致其分解。
在用不同数量的这些DNA对链位培养胚胎小鼠的HeLa细胞和神经元后,他们注意到,添加的DNA位越多,编码SMA蛋白的mRNA水平就越高。其中两个被命名为ASO-A和ASO-B的DNA片段是最有效的。这些实验和其他实验表明,SMN lnc-RNA似乎降低了SMN mRNA的水平,从而阻止了更多的SMN蛋白的生成。
Nusinersen和正在为脊髓性肌萎缩症开发的类似化合物专注于增加或制造更多的SMN基因产物,将其转化为可用的蛋白质。为了观察关闭SMN lnc-RNA是否能增加SMN水平,减缓或阻止脊髓性肌萎缩,研究人员在出生后第一天和第三天向患有严重脊髓性肌萎缩的新生小鼠注射了每公斤400毫克的ASO-A DNA片段。在第10天,研究人员发现治疗小鼠大脑中的SMN lnc-RNA减少了70%,但与注射生理盐水的小鼠相比,存活率、体重和站立能力并没有改善。
fda批准的第一个也是最新的nusinersen治疗方法并不能完全治愈这种疾病,所以Sumner的研究团队想看看使用ASO-A联合nusinersen是否能进一步改善脊髓性肌萎缩小鼠的肌肉形态和功能。Nusinersen也由小段DNA组成,这些DNA改变了smnmrna的加工方式,从而使更多的smnmrna转化为蛋白质。
脊髓性肌肉萎缩的小鼠在出生后第一天注射ASO-A,每公斤剂量低50毫克的单独nusinersen, ASO-A和nusinersen,或生理盐水。每种治疗15只小鼠。联合治疗将平均生存期提高到37天,其中4只小鼠的生存期超过120天。
盐水和ASO-A小鼠平均活了18天,而仅用nusinersen治疗的小鼠平均活了25天。同时服用这两种药物的小鼠也达到了平均水平体重50天后摄入14克只服用nusinersen的老鼠体重没有增加超过6克。没有患病的健康小鼠50天后体重约为20克。
研究人员还测试了小鼠在被放入透明圆柱体后一分钟内后腿直立的次数,这是测试运动能力的标准实验指标。健康的小鼠将养育约6次,接受两种疗法治疗的脊髓性肌肉萎缩小鼠将养育约4次,而单独服用任何一种药物的小鼠仅养育约2次。
Sumner说:“我们还不知道SMN lnc-RNA是否真的在这种疾病中起作用,但它是一个方便的靶点,我们已经利用它来治疗小鼠的脊髓性肌萎缩症。”“我们仍然想确定lnrna是如何发挥作用的,以及何时发挥作用,这将使我们更好地掌握如何更有效地靶向它。”
Sumner说,lnc- rna仍然是一个快速发展的领域,我们才刚刚开始了解它们的作用以及它们在疾病中的作用。
生产nusinersen的Biogen公司将每支nusinersen的价格定在12.5万美元,即第一年的治疗价格约为75万美元。由于脊髓性肌萎缩症是一种罕见的疾病,这种疗法不会大规模生产。
此外,由于药物不能穿过血脑屏障,需要通过脊髓穿刺给药,这需要专门的设施。该药最常见的副作用包括呼吸道感染和便秘,可能会降低血小板水平和肾脏损害。长期或持续的副作用,特别是如果治疗影响神经系统外的其他组织,还有待确定。
更多信息:Constantin d'Ydewalle等人。反义转录本SMN- as1调节SMN的表达,是脊髓性肌萎缩的新治疗靶点神经元(2017)。DOI: 10.1016 / j.neuron.2016.11.033