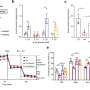
细胞过早分化导致胰腺发育障碍
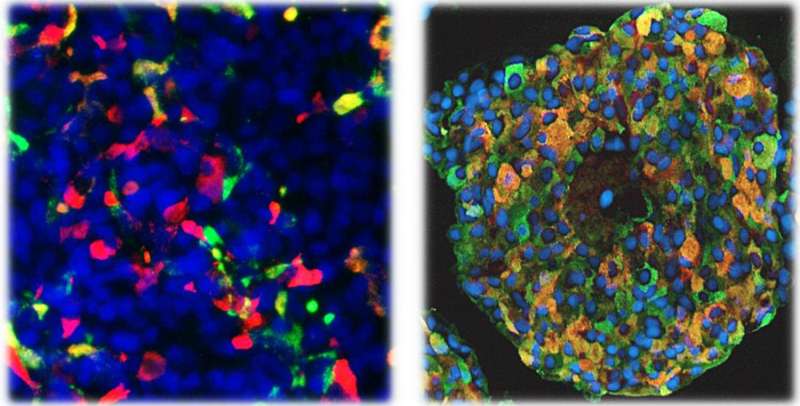
芬兰赫尔辛基大学的研究人员发现了STAT3基因突变导致胰腺发育紊乱和婴儿糖尿病的机制。
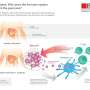
新生儿糖尿病(NDM),或发生于6个月以下婴儿的糖尿病,是一种罕见的糖尿病,由对发育或功能至关重要的基因突变引起β细胞.在大约一半的此类病例中,该病变成了永久性疾病(PNDM)。到目前为止,已有20多个基因的突变被确认为导致新生儿糖尿病的永久性变种。
与1型糖尿病不同,NDM患者通常没有与糖尿病相关的自身抗体。然而,最近发现激活STAT3基因的突变可能导致新生儿糖尿病,包括强烈的自身免疫现象。
最强烈激活STAT基因的突变(K392R)被发现会导致最严重的疾病新生儿糖尿病.这种突变是2014年在一名芬兰患者身上发现的,这名患者出生时β细胞抗体水平很高,胰腺发育不全。该患者后来在不同器官出现多种自身免疫表现。
Timo Otonkoski教授领导的一项新研究,通过诱导检测了STAT3突变对胰腺发育的影响多能干细胞(iPS)来源于患者的皮肤细胞.这项研究发表在细胞的报道.
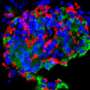
从皮肤细胞中产生的iPS细胞被用来分化成胰岛细胞通过一种复杂的体外方法来反映人类胰腺的正常发育。在分化前,使用CRISPR-CAS9基因组编辑修复患者细胞中的点突变。在此之后,可以比较两种基因相似的细胞在胰腺发育过程中患者细胞的分化情况:一种是携带疾病突变的患病细胞,另一种是通过基因组编辑修复后的健康细胞。
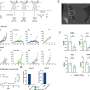
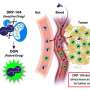
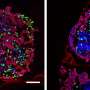
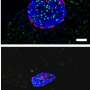
结果显示,患者细胞产生的STAT3蛋白突变导致胰腺祖细胞过早分化为分泌胰岛素或胰高血糖素的内分泌细胞。结果在细胞培养和移植到小鼠的细胞中都很明显,这使得研究人员可以研究细胞时间要长得多。
“我们发现的突变的STAT3蛋白机制的影响解释了胰腺发育不全和糖尿病的早期发作,即使没有自身免疫机制造成的损伤,”博士后研究员和文章的第一作者Jonna Saarimäki-Vire说。
奥通科斯基教授和负责基因组编辑的迭戈·巴尔博亚(Diego Balboa)指出,尽管这种突变很罕见,但这项研究具有更广泛的影响。
“这些结果揭示了之前未知的STAT3基因在胰腺发育中的重要性。我们还成功地使用了新的干细胞技术基因组编辑能够对疾病的机制进行高精度分析的方法突变.我们打算在未来使用同样的方法来研究其他糖尿病基因。”