Rydapt被批准用于成人急性髓系白血病
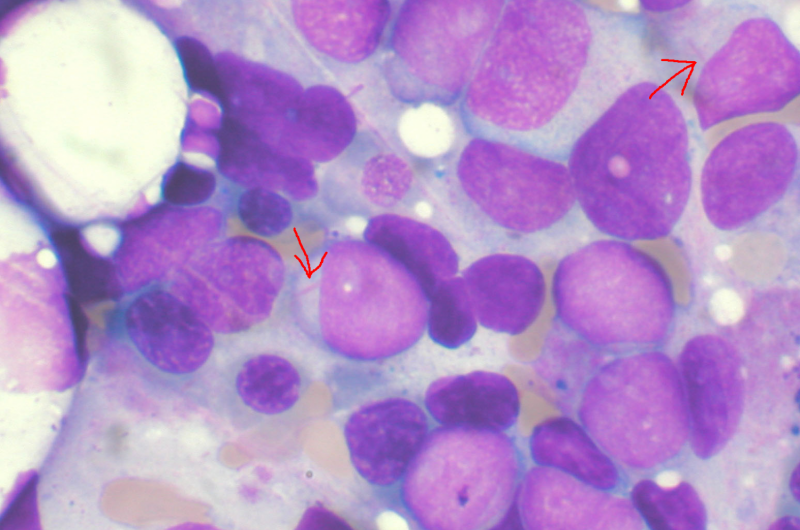
(HealthDay) -Rydapt (midostorin)已被美国食品和药物管理局批准联合化疗,用于治疗患有特定基因突变FLT3的急性髓系白血病(AML)的成年人。
AML,一种在骨髓中形成的快速扩散的癌症白细胞FDA表示,预计每年有不到2万人被诊断患有这种疾病,预计将有超过1万人死于这种疾病。
Rydapt是一类叫做激酶抑制剂它们被设计用来阻止酶的生长癌细胞生长.这项临床研究对700多名以前没有接受过AML治疗的患者进行了评估。常见的副作用包括白细胞计数低、发烧、恶心、头痛和肌肉/骨骼疼痛。更严重的副作用可能包括肺损伤。
FDA说,孕妇或哺乳期女性不应服用Rydapt,因为它可能会伤害正在发育的胎儿或新生儿。
同时批准了一项伴发诊断试验来检测FLT3基因突变。
瑞士制药商诺华制药公司批准了Rydapt。
进一步探索
更多信息:如欲了解更多,请浏览食品及药物管理局.
版权所有©2017每日健康.版权所有。
引用Rydapt获批用于成人急性髓系白血病(2017年4月28日),检索自2021年5月25日//www.pyrotek-europe.com/news/2017-04-rydapt-adults-acute-myeloid-leukemia.html
这份文件受版权保护。除为私人学习或研究目的而进行的公平交易外,未经书面许可,不得转载任何部分。内容仅供参考之用。








用户评论