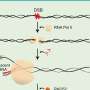
个性化PRRT改善了神经内分泌肿瘤的辐射传递
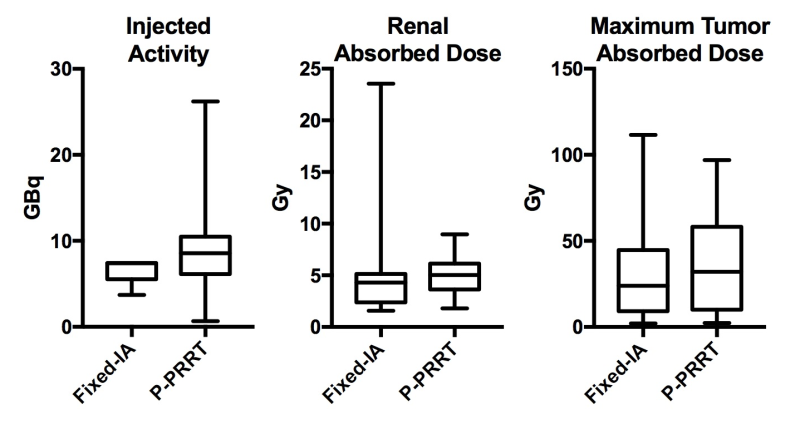
根据核医学和分子成像学会(SNMMI) 2017年年会上发表的研究,神经内分泌癌极其难以管理,不太可能治愈,但研究人员打算通过个性化患者肽受体放射性核素治疗(PRRT)剂量来减缓这些肿瘤的进展,并帮助患者生存。
PRRT已经成为一个治疗是相对罕见和容易被忽视的神经内分泌肿瘤(NETs)的首选。靶向治疗旨在锁定和附着在肽受体阳性肿瘤上,同时保留可能因全身治疗而受损的组织。然而,研究人员仍在完善这种做法。
“到目前为止,大多数PRRT治疗都是一应所有的,这意味着每个患者接受的放射量都是相同的,”Jean-Mathieu Beauregard医学博士说,他是加拿大魁北克省魁北克市Université Laval放射学和核医学系的助理教授。“这导致对器官和肿瘤的吸收辐射剂量变化很大。许多患者可能无法从PRRT中获得最大益处,因为他们最终接受的剂量低于他们的身体实际能承受的剂量。”
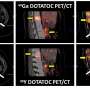
在这项研究中,研究人员使用了一种名为镥-177 (177Lu)-八曲酸,它类似生长抑素生长抑制激素。通常情况下,病人在几个连续的周期内接受固定量的放射性,例如200毫勒。这是第一次177基于精密调谐的SPECT剂量测定法,lu -八曲酸PRRT已经与患者的个体耐受性相匹配,SPECT剂量测定法评估了在肾脏等关键器官中积聚的辐射量。
总共27例神经内分泌癌患者接受了55例个性化治疗177lu -八曲酸循环于2016年4月至12月,随后进行定量SPECT剂量测定。对肾脏的辐射剂量进行量化,以优化给药剂量,同时保持患者的安全和良好的耐受性。在每个治疗周期后的第2周、第4周和第6周,记录副作用,进行血液计数以及肾和肝生化检查。结果显示辐射剂量对大多数参与者的肿瘤的影响增加了三倍于传统PRRT的剂量。此外,严重的副作用和毒性仍然很少与个性化的方法。
未来几个月计划进行更多的研究,以确定个性化PRRT如何改善治疗效果,如减少肿瘤进展和延长生存期。