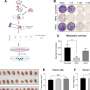
在结直肠癌细胞基因组中逐个编辑基因,发现新的药物靶点
KRAS基因突变导致的癌症是最致命的。几十年来,研究人员一直试图直接靶向KRAS突变蛋白作为治疗肿瘤的手段,但都没有成功。加州大学圣地亚哥分校医学院的研究人员现在没有针对突变的KRAS本身,而是在寻找其他基因或分子,这些基因或分子在受到抑制时,只有当KRAS也发生突变时才会杀死癌细胞。
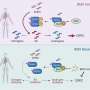
该团队使用CRISPR-Cas9基因编辑技术系统地灭活了人类结直肠基因组中的每个基因癌症KRAS突变和不突变的细胞。他们发现,当两种编码代谢酶的基因nadk和khk也失活时,小鼠体内kras突变的结直肠癌细胞的生长减少了大约50%。
这项研究于9月27日发表于癌症研究,为kras驱动的癌症提供了潜在的新药物靶点。
“我们在实验室中培养的癌细胞并没有得到同样的结果——当NADK和KHK基因失活时,我们看到的生长抑制只发生在哺乳动物系统的肿瘤中,在更现实的微环境中肿瘤必须生存,”资深作者塔里克·拉纳博士说,他是加州大学圣地亚哥分校医学院和摩尔斯癌症中心的儿科学教授。bob电竞“这表明代谢依赖性肿瘤细胞与在活体系统中生长的相同细胞相比,在实验室培养皿中生长可能存在巨大差异,这突出了标准实验室为基础的潜在局限性癌细胞生长测试。”
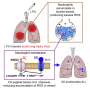
大约20%到30%的人类癌症都有KRAS基因突变。KRAS突变发生在许多最致命和最难治疗的癌症中,包括肺癌、胰腺癌和结直肠癌。KRAS突变癌症细胞能够以一种比正常细胞更有生长优势的方式重组它们的新陈代谢。
Rana治疗kras驱动的癌症的方法——除了kras之外抑制其他基因或分子——被称为“合成致命性”,因为这种干预只对突变细胞致命。在一个之前的研究Rana的团队使用microRNAs(小块遗传物质)文库系统地阻断蛋白质的产生,并寻找那些与KRAS突变结合后合成致命的抑制物。
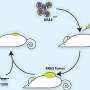
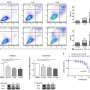
在他们最新的研究中,Rana的团队使用CRISPR-Cas9系统地灭活了两种人类结直肠癌细胞系中的基因,其中一种具有正常的KRAS,另一种具有突变的KRAS。然后,他们测试了这些细胞系在小鼠体内生长成肿瘤的能力。他们发现,使两种代谢酶NADK和KHK失活,可以使KRAS突变肿瘤的生长减少约50%,但对正常KRAS肿瘤没有影响。他们还用市面上可以买到的小分子抑制剂阻断了这些酶,只在小鼠的肿瘤中看到了肿瘤生长的显著减少细胞突变KRAS。
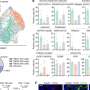
Rana和他的团队还发现了几个新的基因,当它们失活时,会产生相反的效果——它们会增加KRAS突变肿瘤的生长,但不会增加正常KRAS肿瘤的生长。这些类型的基因被称为“肿瘤抑制因子”,因为它们通常会抑制癌细胞的生长。
“我们研究中最令人惊讶的发现之一是,在哺乳动物微环境中直接进行这种类型的遗传筛查,不仅揭示了新的合成致命相互作用,而且还揭示了新的肿瘤抑制因子基因依赖于KRAS突变,”第一作者Edwin Yau医学博士说,他是Rana实验室的血液学/肿瘤学和癌症治疗学培训计划研究员。
其中一个新的肿瘤抑制基因编码INO80C, INO80C是一种大型多亚基蛋白,除其他外,它可以稳定基因组。Rana、Yau和同事们现在正在采取措施推进他们的发现,最终目标是更好地了解kras突变癌症是如何发展的,并将这些见解转化为开发新的治疗方法来阻止它们。
更多信息:癌症研究(2017)。DOI: 10.1158 / 0008 - 5472. - 17 - 2043