癌症研究人员开发新的战略目标KRAS突变
尽管喀斯特是一个主要的致癌基因与侵略性的癌症有关,药物阻止喀斯特作用没能阻止癌症恶化在临床设置。直到现在,喀斯特一直臭名昭著的无药可治”。”
在一项新的研究中,在本月出版癌症的发现加州大学圣地亚哥医学院的研究人员报告说,大约一半的肺和胰腺癌的KRAS突变,产生上瘾的基因,因为它们的进展。通过理解的机制,导致这些癌症仍依赖于喀斯特生存,他们能够确定药物针对它的能力。
“某些肿瘤使用KRAS基因突变来提高他们的生存,帮助他们吸收营养和毒素过程,使它们对喀斯特上瘾,”David Cheresh说博士,加州大学圣地亚哥分校医学院的病理学和资深作者的特聘教授。“其他的肿瘤不使用喀斯特这样可以没有它,即使它是需要启动癌症。基于生物标志物,我们发现,我们现在知道,癌症会上瘾,不会。”
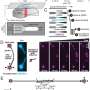
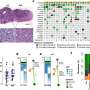
目前没有有效的治疗胰腺癌的95%和30%的非小细胞肺癌有KRAS突变。蛋白质的研究小组的研究人员发现,绑定Galectin-3细胞表面受体整合素avb3放大优势由KRAS基因突变,创造一个独特的脆弱性,可以与现有的有针对性的药物。
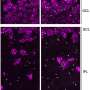
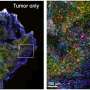
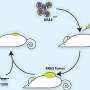
Cheresh和团队发现一个叫做gcs Galectin-3抑制剂- 100能够杀死KRAS-addicted细胞在体外和停止KRAS-addicted肿瘤进展的小鼠模型。重要的是,他们发现一个肿瘤只能应对药物如果是积极整合素αvb3。
“这可能是第一批成功目标KRAS突变的癌症的方法。以前,我们不明白为什么只有某些KRAS-initiated癌症仍将沉溺于突变,“创新和产业联盟副主任Cheresh说加州大学圣地亚哥穆尔斯癌症中心。“现在,我们明白,整合素的表达αvb3创建喀斯特瘾。那些上瘾的癌症,我们觉得最容易使用Galectin-3抑制剂针对这个途径。”
打断这一途径可能是更有前途的起源比试图阻止个人KRAS-driven功能,研究人员写道。考虑到KRAS-addicted癌症被发现是高度敏感Galectin-3抑制剂在临床前模型,下一步将是目前临床测试Galectin-3抑制剂在病人的肿瘤表达KRAS基因突变和αvb3相关生物标志物预测的反应。
“KRAS突变影响大量的癌症患者。如果病人有KRAS突变的癌症,癌症也是αvb3阳性,那么治疗的患者可能是一个候选目标这个途径,“Cheresh说。“我们的研究表明一个个性化医学的方法来识别和利用喀斯特上瘾肿瘤,阻止肿瘤的进展提供了新的机会,目前没有可行的有针对性的治疗选择。”
更多信息:莱提纱·赛甘·et al, Galectin-3制药KRAS-addicted癌症的脆弱性,癌症的发现(2017)。DOI: 10.1158 / 2159 - 8290. - cd - 17 - 0539