2017年9月15日报告
新技术结合起来鉴定了一种癌症背后的特定DNA缺陷
来bob游戏自荷兰和英国的一组研究人员开发了一种研究遗传类型癌症的技术,使用两种相对较新的技术——类器官发育和CRISPR/Cas9。在他们发表在杂志上的论文中科学,该团队描述了他们的技术,以及如何将其用于更好地了解某些类型的遗传性癌症。
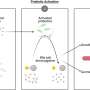
为了更好地了解由于遗传特征而形成肿瘤的因素,研究人员从人类中创造了类器官肠干细胞.类器官是由细胞和组织组成的类似器官的构造物,它们是为了在活体组织上进行实验而人工生长的,而这些实验无法在真正的器官上进行。这个场景中的类器官是为了肿瘤的遗传研究而生长的。
这项研究包括使用CRISPR/Cas9从类器官细胞中切割一种名为NTHL1的基因。NTHL1在人类结肠中自然存在。从类器官的DNA中切割它的目的是为了发现这样做是否会导致与真正的癌症患者相似的遗传特征。
在正常情况下,NTHL1产生的蛋白质是切除缺陷的过程的一部分基因.通过移除基因瀑样研究人员发现,出现了一种突变特征,与一名此前未知类型的乳腺癌患者的突变特征相似。对患者遗传史的研究揭示了一种遗传种系,导致NTHL1基因失活,进而导致肿瘤生长。这意味着这项技术已经确定了一种与特定类型的遗传性癌症相关的基因缺陷。
通过使用联合技术来识别潜在的可遗传癌症形式,研究人员证明,这是一种可行的研究方法,可以更好地理解遗传DNA修复缺陷在遗传性癌症发展中的作用。他们认为,它也可以用来更好地理解环境诱变剂所涉及的过程。他们还指出,他们的研究表明,现在有可能通过对发育的肿瘤的DNA进行测序来检测遗传形式的癌症癌症病人.
进一步探索
摘要
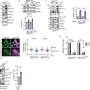
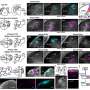
突变过程是癌症发生和发展的基础。这些过程在癌症基因组中的特征可以解释癌症的病因,并具有诊断和预后价值。在这里,我们开发了一种策略,可用于探索癌症相关突变特征的起源。我们使用CRISPR/Cas9技术删除了人类结肠类器官中的关键DNA修复基因,随后进行了延迟亚克隆和全基因组测序。我们发现错配修复基因MLH1缺陷类器官的突变积累是由复制错误驱动的,并准确模拟了在错配修复缺陷的结直肠癌中观察到的突变特征。将这一策略应用于癌症易感基因NTHL1(编码碱基切除修复蛋白),揭示了先前在乳腺癌队列中观察到的突变足迹(签名30)。我们发现签名30可能源于种系NTHL1突变。
©2017 Mbob游戏edical Xpress