饥饿肿瘤:新靶点发现
活跃生长的肿瘤对氧气和营养物质的需求很高。因此,它们通过一个叫做血管生成的过程刺激血管的生长。如果抑制肿瘤相关血管生成,可能会限制肿瘤生长。来自德国癌症研究中心和海德堡大学欧洲血管科学中心的科学家现在发现了一种抗血管生成肿瘤治疗的新靶点。他们发现,小鼠体内一种信号分子的缺失会导致晚期肿瘤血管的形成减少。这延缓了癌细胞的生长并限制了转移的形成。
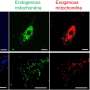
癌细胞,像所有细胞一样,需要营养和氧气,这些营养和氧气由血管.由于癌细胞分裂得特别快,所以新的血管需要以不受控制的方式迅速生长进入血管肿瘤.阻止这一进程可能会限制肿瘤的生长.赫尔穆特·奥古斯丁实验室的科学家们现在已经证明,受体Tie1在血管生成中起着至关重要的作用。Tie1表示为内皮细胞即排列在所有血管内部的细胞。Tie1与其他信号分子相互作用,从而控制血管的生长。
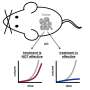
Tie1在肿瘤血管系统中过表达。这有助于血管的生长,并使肿瘤生长。令人惊讶的是,Tie1的促生长作用仅发生在肿瘤生长的后期。在内皮细胞不能表达Tie1的基因工程小鼠中,肿瘤生长最初没有改变。然而,两周后,当肿瘤生长到相当大的尺寸时,没有Tie1的小鼠的生长速度明显放缓。这可能是Tie1作为治疗靶点的后期临床开发的一个优势:“肿瘤大多是在其进化已经相当深入的时候被诊断出来的,”Augustin解释说。“因此,如Tie1所示,识别在肿瘤生长后期活跃的治疗靶点尤为重要。”
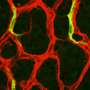
针对Tie1有另一个积极的影响:它稳定的墙壁血血管,从而防止转移的形成。转移是导致大多数癌症死亡的原因。这种继发性肿瘤发生时癌症细胞离开原发肿瘤,进入血液,然后到达远处的器官。它们可以在次要部位休眠数周甚至数年,然后再次开始分裂形成转移。该研究的首席科学家西尔维亚·拉·波特解释说:“我们从基因上删除了Tie1,以阻止肿瘤的生长和转移。”“接下来,我们将研究用药物阻断Tie1是否具有同样的有益效果。”
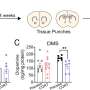
研究表明,手术切除后原发肿瘤, 14只正常对照小鼠中有10只发生转移。在没有Tie1的小鼠中,14只动物中只有1只发生转移。
Tie1的确切作用机制仍是深入研究的课题。这种分子是所谓的孤受体,这意味着它是一种没有已知结合伴侣的受体。未来的研究需要阐明铁一的神秘功能。
阻断血管生成的概念并不新鲜。2004年,药物Bevacizumab (Avastin)获得临床批准。它通过阻断血管生成因子来限制肿瘤生长增长因子(VEGF)。然而,贝伐珠单抗的疗效有限。这就是为什么科学家们正在大力研究第二代抗血管生成靶点,这些靶点可以用于联合治疗,以提高抗血管生成干预的疗效。
近年来,制药行业对作为治疗靶点的Angiopoietin2进行了深入研究。然而,血管生成素2阻断药物的临床研究结果令人失望。与Tie1不同,Ang2主要影响肿瘤发展的早期阶段,这可能是其临床疗效有限的原因之一。鉴于Tie1靶向不同的治疗窗口,未来的研究将需要证明它是否能被证明是一种更好的治疗方法治疗目标.
更多信息:Silvia La Porta等,内皮tie1介导的血管生成和血管异常促进肿瘤进展和转移,临床研究杂志(2018)。DOI: 10.1172 / JCI94674