胎儿的肠道组织的细胞模型可以帮助对抗致命的新生儿疾病
细胞模型产生的胎儿和成人肠组织调查人员从黏膜免疫学和生物学研究中心(MIBRC)大众婴幼儿专科医院的儿童(MGHfC)已经确定了免疫应答的差异自然肠道细菌在不同发育时期。研究结果在线发表的一篇论文中描述细胞和分子胃肠病学和肝脏病学,支持该模型的使用调查条件包括坏死性小肠结肠炎(NEC),一个危险的影响早产儿胃肠道疾病。
NEC可以摧毁一个婴儿的肠道壁,导致穿孔、感染甚至死亡。条件不利影响最小的婴儿,30 - 50%的死亡率很低和极低出生体重儿童。即使孩子幸存,并发症可能需要手术来移除受损的肠段,从而影响孩子的许多方面发展,导致许多孩子的生活质量。
数十年的研究并没有导致有效的治疗或预防NEC,虽然只喂养早产儿母乳可以减少风险。在动物模型的研究并没有完全打开的细胞和分子机制导致NEC的发作,但研究表明,异常响应gut-colonizing细菌可能发挥作用在为其发展创造条件。
“人类模型的缺乏阻碍了研究NEC,”塞法萨诺说,医学博士,主任MGHfC MIBRC,哈佛医学院的儿科教授,文章的第二作者目前的报告有前景的新模型来研究肠道婴儿发展。bob电竞
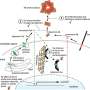
用人类肠道样本,MIBRC科学家培养肠道“瀑样”胎儿和成人发展的不同阶段。这些多细胞集群,由从小肠上皮细胞,使研究人员研究“mini-gut”应对殖民细菌在不同的发展时期。和时间在NEC的发展似乎是至关重要的。
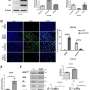
“在最不成熟的婴儿,我们认为不成熟肠上皮细胞创建一个夸张的同桌的肠道细菌的免疫反应,导致NEC的发病机制,”普圣吉博士说,这项研究的第一作者。她和她的同事分析了基因表达模式的胎儿和成人肠道瀑样,发现胎儿瀑样集群大致分成两组根据他们的发育年龄:早期(大约14 - 15周)和晚期(约17 - 22.5周)。当暴露于gut-colonizing细菌或木糖醇时,两组有不同的免疫反应的基础上发展时代。
“这表明只有胎儿瀑样从成熟的胎儿可能会对细菌作为早产儿,“圣吉说。“所以得出结论从分析年轻胎儿组织可能会误导。”
艾伦·沃克博士前MIBRC主任和研究的文章的第二作者,说,“NEC是一种疾病最好由预防、处理的肠早产儿并不具备处理细菌在母亲的子宫。”A prominent pediatric gastroenterologist and investigator into the field of NEC research, Walker calls this a "breakthrough moment" into the causes of the devastating disease.
“这项工作我们更接近开发patient-derived移动,体外模型。这种方法的优点是,我们可以建立一个库组织的胎儿和婴儿发育的不同阶段。一旦你进行观察时,你可以去biorepository并使用瀑样组织测试,观察,“沃克说,他是胖的哈佛医学院儿科教授。bob电竞
这部小说研究模型具有广泛的应用潜力。“这不仅有前途的新模型人类的肠道瀑样让我们研究这个毁灭性的疾病,它还提供了新的工具来了解婴儿肠道发育,“圣吉说,他是一个遗传学家背景的干细胞和粘膜生物学和哈佛大学医学院的儿科的教练。bob电竞球队现在计划从婴儿肠道瀑样组织文化受到NEC确定炎症导致疾病的机制。
“这重要的工作才可能由于在MIBRC高度协作环境,“圣吉补充道。”沃克博士的团队为我们提供了指导和专业知识在胎儿肠道发育和NEC发病机理。阻止这种疾病非常重要的工作。我们希望开发战略,以防止NEC的表达才能立足在任何婴儿的肠。”
更多信息:美国圣吉et al,人类fetal-derived enterospheres提供肠道发展见解和新颖的模型来研究坏死性小肠结肠炎(NEC),细胞和分子胃肠病学和肝脏病学(2018)。DOI: 10.1016 / j.jcmgh.2018.01.014